Biohemija
Biokemija ili biohemija je kemija života, most između biologije i kemije koji proučava kako kompleksne hemijske reakcije stvaraju život. Biohemija je hibridni deo hemije koji konkretno proučava hemijske procese u živim organizmima.[1] Ovaj članak diskutuje samo kopnenu biohemiju, koja počiva na ugljeniku i vodi. Kako svi oblici života koje danas imamo na planeti imaju zajedničko poreklo, prema tome imaju i slične biohemije, kao što su genetska šifra i stereohemija mnogih biomolekula. Nepoznato je da li su naizmenične biohemije uopšte i moguće.[2][3]
Biohemija proučava strukturu i funkciju celularnih komponenti, kao što su proteini, ugljeni hidrati, lipidi, nukleinske kiseline i ostali biomolekuli. Iako postoji ogroman broj različitih biomolekula, oni se često sastoje od istih jedinica koje se ponavljaju monomera, ali koji se ponavljaju u različitim sekvencima. Nedavno, biohemija je počela da se fokusira na proučavanje reakcija u kojima su katalizatori enzimi, i na proučavanje osobina proteina.
Biohemija metabolizma ćelije i biohemija endokrinog sistema su dva domena koja su intezivno studirana. Druge oblasti koje spadaju pod pojam biohemije su genetska šifra (DNK, RNK), sinteza proteina, transport kroz ćelijsku membranu i transdukcija signala.
Razvoj biohemije[uredi | uredi kod]

U početku se verovalo da na žive materije zakoni nauke deluju drugačije od tzv. neživih materija. Verovalo se da samo živa bića mogu da proizvedu molekule života (od prethodno postojećih živih molekula). Međutim 1828 Fridrih Voler je objavio stručni rad koji je za temu imao sintezu uree, pritom dokazavši da organska jedinjenja mogu biti stvorena veštačkim putem.[5][6]
Početkom biohemije se najčešće uzima za trenutak kada je pronađen prvi enzim, diastaza, 1833 od strane Anselma Pajena. Veruje se da je 1903 nemački naučnik Karl Nojber dao nauci današnje ime biohemija. Od tada biohemija je naveliko napredovala, naročito tokom sredine 20-tog veka, sa otkrićem i razvojem metoda kao što su hromatografija, rentgentska difrakcija, nuklearna magnetna rezonanca- NMR, radioizotopsko obeležavanje, elektronska mikroskopija i simulacija molekularne dinamike. Zahvaljujući ovim metodima naučnici su otkrili i detaljno analizirali mnoge molekule kao i aktivnosti u samim ćelijama na molekularnom nivou kao što su putevi metabolizma u ćelije, tj glikoliza i Krebsov ciklus (takozvani ciklus limunske kiseline).
Danas, otkrića u oblasti biohemije se koriste u mnogim stručnim oblastima, od genetike i molekularne biologije do poljoprivrede i medicine. Prva upotreba biohemije je najverovatnije bila pre 5000 godina pravljenjem hleba koristeći kvasac.
Okvir proučavanja[uredi | uredi kod]
Biohemija se bavi:
- proučavanjem strukture biomolekula: kako su one građene, kakva je molekularna organizacija nekog organizma, kako molekularne jedinice nastaju i kako jedne s drugim reagiraju.
- proučavanjem razmjene materija: kako se određene supstance mijenjaju djelovanjem živih bića, koje bioenergetske pretpostavke su neophodne za to, koji biokatalizatori su uključeni, kako djeluju određeni mehanizmi pretvaranja supstanci i kako se razmjena materija upravlja i kontrolira.
- proučavanjem razmjene informacija unutar nekog organizma kao i između organizama; kako se informacije skladište, pozivaju i dalje prosljeđuju, kako se koordiniraju različiti sistemi unutar neke ćelije, između različitih ćelija i između organizama.
U tom aspektu, ona se koncentrira na proučavanja određenih klasa supstanci kao što su nukleinske kiseline, bjelančevine, masti, ugljikohidrati kao i njihovi derivati, a one se općenito nazivaju i biomolekule. Pretežni dio biohemijski važnih procesa odigravaju se unutar živih bića odnosno u pretežno vodenom okruženju.
Metode[uredi | uredi kod]
U biohemiji se primjenjuju brojne metode iz različitih oblasti. Klasična biohemija najviše se oslanja prvenstveno na analitički hemiju, organsku hemiju, fizikalnu hemiju i fiziku. Pri tom su među najvažnijim tehnikama u biohemiji u upotrebi (ultra-)centrifugiranje, SDS-gel-elektroforeza, hromatografija, elektroforeza, spektroskopija, radioaktivno obilježavanje (radioaktivni traser, marker), izotopske tehnike, kristalizacija, potenciometrijske, elektrometrijske, polarografske i manometrijske tehnike i druge. Posljednjih nekoliko godina do izražaja su došle i molekularnobiološke metode i metode iz oblasti informatike, mikrobiologije i drugih oblasti. Također, u modernoj biohemiji koriste se kvantitativna mjerenja i analize rezultata matematičkim metodama i postavljanje formalnih teorija pomoću matematike.
Podela[uredi | uredi kod]
U zavisnosti od načina posmatranja, dio biohemije koja se bavi bolestima čovjeka naziva se medicinska biohemija. Dalje, postoji i ekobiohemija koja se bavi ekosistemima. Biljna biohemija proučava biljke, dok imunološki sistem proučava imunologija, a neurohemija se bavi nervnim sistemom.
Također, prema grupama hemijskih spojeva biohemija se može podijeliti naprimjer na hemiju bjelančevina, biohemiju nukleinskih kiselina, biohemiju ugljikohidrata te biohemiju masti. Hemija prirodnih supstanci obuhvata grupu malih molekula. Enzimologija i provođenje signala (trandukcija) predstavljaju posebni fokus izučavanja biohemije. Biofizikalna hemija proučava biomolekule i živa bića metodama fizikalne hemije.
Biomolekuli[uredi | uredi kod]
U biohemiji se javljaju četiri glavne klase molekula (često zvanih biomolekuli): ugljeni hidrati, lipidi, proteini, i nukleinske kiseline. Mnogi biološki molekuli su polimeri: u toj terminologiji, monomeri su relativno mali molekuli koji se vezuju jedan za drugi i kreiraju velike makromolekule poznate kao polimeri. Kad se monomeri povezuju pri sentizi bioloških polimera, oni podležu procesu koji se zove dehidraciona sinteza. Različiti makromolekuli mogu da formiraju veće komplekse, koji su obično neophodni za biološku aktivnost.
Karbohidrati[uredi | uredi kod]
Funkcije karbohidrata su skladište energije i struktura. Šećeri su karbohidrati, međutim postoje i karbohidrati koji nisu šećeri. Na Zemlji karbohidrati su najrasprostranjeniji biomolekuli. Najjednostavniji karbohidrat je monosaharid, koji se između ostalog sastoji od ugljenika, vodonika, i kiseonika, u odnosu 1:2:1 sa generalnom formulom CnH2nO gde je n najmanje 3. Glukoza, jedan od najbitnijih karbohidrata, je primer monosaharida. Kao i fruktoza, šećer koji daje voću sladak ukus.
Dva monosaharida mogu biti spojena zajedno pomoću dehidracije, reakcije u kojoj se na svaka dva spojena monosaharida dobija jedan molekul vode. U toj reakciji sa jednog monosaharida se otkida jedan atom vodonika, a sa drugog monosaharida se otkida hidroksilna grupa (-OH) i takva dva monosaharida se spoje, dok se njihovim spajanjem dobija jedan molekul vode H—OH tj. H2O. Novonastali molekul od sva monosaharida se sada naziva disaharid. Obrnuti proces, stvaranje dva monosaharida od jednog disaharida se naziva hidroliza kada molekul vode napadne vezu između dva spojena šećera. Napoznatiji disaharid je saharoza, obični šećer, koji se u naučnom kontekstu zove kuhinjski šećer kako bi se razlikovao od ostalih šećera. Saharoza se sastoji od molekula glukoze i molekula fruktoze. Drugi važan disaharid je laktoza, koji se sastoji od spojenih molekula glukoze i galaktoze. Većina ljudi sa godinama smanjuje proizvodnju enzima laktaze koji pomoću reakcije hidrolize razdvaja laktozu u monosaharide, glukozu i galaktozu. Rezultat smanjivanja broja laktaze u organizmu dovodi do netolerancije laktoze, odnosno u toj starosnoj grupi ljudi sa smanjenjim brojem enzima ne mogu da piju mleko i mlečne proizvode.
Kada se nekoliko, 3 do 6, monosaharida spoje, taj lanac molekula se zove oligosaharidi (oligo znači više). Ovi molekuli se često koriste kao markeri i signali, ali imaju i druge uloge.
Mnogi monosaharidi spojeni zajedno nazivaju se polisaharidima. Oni mogu biti spojeni zajedno u jednom dugom linearnom lancu, ili mogu biti razgranati. Dva najčešća polisaharida su celuloza i glikogen, oba se sastoje od ponavljajućih monomera glukoze. Biljke stvaraju celulozu koja je važna strukturna konponenta ćelijskog zida. LJudska bića niti mogu da proizvedu celulozu niti mogu da je vare. Glikogen je karbohidrat koji ljudi i životinje koriste kao skladište energije.
Glukoza je važan izvor energije u većini oblika života. Veliki broj kataboličkih procesa( videti katabolizam)je moguć zahvaljujući glukozi. Glukoza se upotrebljava u jednom veoma važnom procesu -glikoliza, u kojem je cilj da se od jednog molekula glukoze dobiju dva molekula piruvata, iz čega sledi produkcija dva molekula ATP-a, energija ćelije, zajedno sa dva reduktovana ekivalenta u formi NAD-a koji se pretvara u NADH. Ovaj proces ne zahteva kiseonik. Ako kiseonik nije dostupan NADH se prebaci u prvobitan oblik, NAD; konvertovanjem pirivata u laktat (kod čoveka na primer) ili u etanol (kod gljiva).
U aerobnim ćelijama sa dovoljno kiseonika, kao mnoge ljudske ćelije, piruvat dalje može biti predmet procesa metabolizma. Pirivat se može promeniti (međutim ova reakcija nije povratna) u acetil-CoA, dajući pritom jedan ugljenikov atom kao nusprodukat ugljen-dioksida, pritom stvarajući još jedan molekul ATP-a i redukujući još jedan NAD (NAD u NADH). Dva molekula acetil-CoA (dobijenih od jednog molekula glukoze) se zatim uključuju u Krebsov ciklus, pritom stvarajući još dva molekula ATP-a, 6 molekula NADA i dva molekula FADH2. Ukupan broj molekula ATP-a koji se dobija ovim putem je 32. Jasno se vidi iz ovoga da kompletna okisdacija glukoze omogućava organizam sa mnogo energije, i iz toga sledi da se kompleksan život na Zemlji pojavio tek onda kad je atmosfera u sebi imala velike količine kiseonika.
Kod kičmenjaka, npr. ljudi, kontraktovanjem mišića, na primer tokom trčanja, dizanja tegova, brzog hoda, organizam ne dobija dovoljno kiseonika kako bi održao nivo energije kako bi ove radnje bile uopšte i moguće. Kada dođe to tog slučaja onda se ćelije prebacuju sa aerobnog metabolizma (kad je kiseonik dostupan) u anaerobni metabolizam (kad kiseonik nije dostupan) i pretvajaru glukozu u laktat, laktičku kiselinu. Jetra može da regeneriše glukozu, procesom glukoneogeneze.
Proteini[uredi | uredi kod]
Glavni članak: Protein
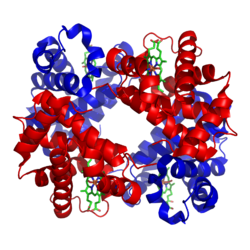
Kao i gore navedeni ugljeni hidrati, neki proteini imaju isključivo strukturnu ulogu. Na primer, kretanje proteina kao što su aktin i miozin omogućavaju kontraktovanje mišića. Jedna od bitnih osobina proteina je njihova specifičnost, što znači da se vezuju samo na određene molekule i jedinjenja. Takva vrsta proteina su antitela. Antitela se vezuju samo za određene molekule. Ova specifičnost proteina je veoma korisna u dijagnostici, ako ne i jedini način dijagnostike. Test ELISA je jedan od testova korišćen kako bi se detektovalo prisustvo HIV virusa, virusa odgovornog za sidu. Kako su antitela specifična, ona se vezuju samo za biomolekule koji se pojavljuju u telu kada je pacijent već oboleo od virusa side. Kada se vrši testiranje sa testom ELISA, ako se utvrdi prisutnost određenih antitela koja se vezuju za biomolekule HIV virusa, onda sa sigurnošću možemo da kažemo da osoba ima HIV virus.
Jedan od najvažnijih vrsta proteina su enzimi. Enzimi su prirodni katalizatori, i imaju veliku ulogu u kinetici bioloških reakcija, tj prema potrebi mogu da ubrzaju ili uspore reakciju. Veoma su specifični, i vezuju se za samo unapred određene biomolekule.
Protein je lanac napravljen od amino kiselina. Amino kiselina se sastoji od ugljenikovog atoma koji je povezan za četiri grupe. Jedna grupa je Amino grupa, —NH2, druga grupa je karboksilna kiselina, —COOH, treća grupa je jednostavan vodonikov atom, -H, i četvrta grupa se obeležava sa -R i po toj grupi se amino kiseline razlikuju jedna od druge. Amino kiseline su povezane peptidnim vezama.
Lipidi[uredi | uredi kod]
Glavni članak: Lipidi Lipidi su jedinjenja koja imaju različite uloge i osobine, a jedna od bitnijih osobina je da su nepolarni, mada ima i veliki broj polarnih lipida. Pod polarnim se podrazumeva da imaju afinitet ka vodi, tj da su hidrofilni, dok nepolarni lipidi znače da nemaju afinitet prema vodi i da su hidrofobni. Poznati lipidi su vosak, fosfolipidi, glikolipidi, terpenoidi i steroidi. Mogu biti cirkularnog ili linearnog oblika, kao i fleksibilni ili rigidni.
Nukleinska kiselina[uredi | uredi kod]
Glavni članak: Nukleinska kiselina Nukleinska kiselina je kompleks biohemijskih makromolekula visoke molekularne mase koji se sastoji od nukleotidnih lanaca koji prenose genetičke informacije.[7] Najpoznatije dve nukleinske kiseline su Dezoksiribonukleinska kiselina DNK i Ribonukleinska kiselina RNK. Nukleinske kiseline se nalaze u svim živim ćelijama i virusima.
Nobelovci iz oblasti biohemije[uredi | uredi kod]
U donjoj galeriji prikazani su neki od najznačajnijih naučnika, dobitnika Nobelove nagrade za istraživanja u oblasti biohemije (ili neke od srodnih disciplina):
-
Hermann Emil Fischer dobio je 1902. Nobelovu nagradu za hemiju za svoj rad iz oblasti šećera i purina.
-
Biohemičar Otto Fritz Meyerhof zajedno Hillom dobio je 1922. Nobelovu nagradu za istraživanja o razmjeni materija u mišićima.
-
Otto Warburg je 1931. dobio Nobelovu nagradu za "otkriće prirode i funkcije fermenata disanja". Stoga je "Medalja Otto Warburg" najvažnije odlikovanje u području biohemije u Njemačkoj.
-
Gerty i Carl Cori zajedno sa Bernardo Alberto Houssayom dobili su 1947. Nobelovu nagradu za svoje biohemijske radove o metabolizmu šećera.
-
Za otkriće ciklusa limunske kiseline Hans Adolf Krebs dobio je Nobelovu nagradu 1953.
-
James D. Watson dobio je Nobelovu nagradu 1962. za svoje istraživanje o DNK.
Biohemičar[uredi | uredi kod]
Studije[uredi | uredi kod]
U većini evropskih zemalja postoje studijski odsjeci za biohemiju u tri stepena: diplomski, postdiplomski (magistarski) i doktorski. U Njemačkoj su diplomski studiji 2008. postepeno zamijenjeni uzastopnim magistarskim i doktorskim studijama:
- U redovnom studiju, dodiplomski stepen ima 9 ili 10 semestara, a najduže od 13 do 14 semestara te nakon njega student stiče titulu diplomirani biohemičar.
- Na magistarskom studiju, studij traje 6 do 8 semestara te nakon njega osoba stiče titulu magistar biohemijskih nauka.
- Doktorski studij po pravilu trajue 3 do 4 semestra, te nakon njega se dobija titula doktor biohemijskih nauka.
Specijalistički studije biohemije[uredi | uredi kod]
U Nemačkoj postoji mogućnost da studenti nakon završetka medicinskog studija pohađaju specijalistički studij za biohemiju (njem. Facharzt). Za to je neophodna još jedna godina daljnjeg studija. Na to se još dodaje i jedna godina studiranja internističke medicine ili pedijatrije.
Na dan 31. decembar 2010. u Nemačkoj su bila registrirana 102 specijalista za biohemiju. Od njih 52 nisu vršila doktorsku praksu. U toku decenije od 2000. do 2010. broj registriranih stručnih medicinskih biohemičara smanjen je za gotovo 50%.
Reference[uredi | uredi kod]
- ↑ Donald Voet, Judith G. Voet (2005). Biochemistry (3 izd.). Wiley. ISBN 978-0-471-19350-0.
- ↑ Metzler, David Everett; Metzler, Carol M. (2001). Biochemistry: The Chemical Reactions of Living Cells. 1. Academic Press. str. 58. ISBN 978-0-12-492540-3.
- ↑ Sen, Chandan K.; Roy, Sashwati (2007). „miRNA: Licensed to kill the messenger”. DNA Cell Biology 26 (4): 193–194. DOI:10.1089/dna.2006.0567. PMID 17465885.
- ↑ Edwards K.J., Brown D.G., Spink, N., Skelly J.V., Neidle S. (1992). „Molecular structure of the B-DNA dodecamer d(CGCAAATTTGCG)2. An examination of propeller twist and minor-groove water structure at 2.2 A resolution”. J.Mol.Biol. 226: 1161-1173. PMID 1518049.
- ↑ Ben-Menahem, Ari (2009). Historical Encyclopedia of Natural and Mathematical Sciences. Springer. str. 2982. ISBN 978-3-540-68831-0.
- ↑ Kauffman, G.B.; Chooljian, S.H. (2001). „Friedrich Wöhler (1800–1882), on the bicentennial of his birth”. The Chemical Educator 6 (2): 121–133. DOI:10.1007/s00897010444a.
- ↑ Krebs, Jocelyn E.; Goldstein, Elliott S.; Lewin, Benjamin; Kilpatrick, Stephen T. (2012). Essential Genes. Jones & Bartlett Publishers. str. 32. ISBN 978-1-4496-1265-8.
Literatura[uredi | uredi kod]
- Fromm, Herbert J.; Hargrove, Mark (2012). Essentials of Biochemistry. Springer. ISBN 978-3-642-19623-2.
- Hunter, Graeme K. (2000). Vital Forces: The Discovery of the Molecular Basis of Life. Academic Press. ISBN 978-0-12-361811-5.
- Tropp, Burton E. (2012). Molecular Biology (4th izd.). Jones & Bartlett Learning. ISBN 978-1-4496-0091-4.
- Molekularna Genetika, Džejms D. Votson, 2005, ISBN 0-8053-4642-2
- Calladine, Chris R.; Drew, Horace R.; Luisi, Ben F.; Travers, Andrew A. (2003). Understanding DNA: the molecule & how it works. Amsterdam: Elsevier Academic Press. ISBN 0-12-155089-3.
- Dennis, Carina; Julie Clayton (2003). 50 years of DNA. Basingstoke: Palgrave Macmillan. ISBN 1-4039-1479-6.
- Horace Freeland Judson 1979. The Eighth Day of Creation: Makers of the Revolution in Biology. Touchstone Books, ISBN 0-671-22540-5. 2nd edition: Cold Spring Harbor Laboratory Press, 1996 paperback: ISBN 0-87969-478-5.
- Olby, Robert C. (1994). The path to the double helix: the discovery of DNA. New York: Dover Publications. ISBN 0-486-68117-3., first published in October 1974 by MacMillan, with foreword by Francis Crick;the definitive DNA textbook,revised in 1994 with a 9 page postscript
- Micklas, David. 2003. DNA Science: A First Course. Cold Spring Harbor Press: ISBN 978-0-87969-636-8
- Ridley, Matt (2006). Francis Crick: discoverer of the genetic code. Ashland, OH: Eminent Lives, Atlas Books. ISBN 0-06-082333-X.
- Olby, Robert C. (2009). Francis Crick: A Biography. Plainview, N.Y: Cold Spring Harbor Laboratory Press. ISBN 0-87969-798-9.
- Rosenfeld, Israel. 2010. DNA: A Graphic Guide to the Molecule that Shook the World. Columbia University Press: ISBN 978-0-231-14271-7
- Schultz, Mark and Zander Cannon. 2009. The Stuff of Life: A Graphic Guide to Genetics and DNA. Hill and Wang: ISBN 0-8090-8947-5
- Gunther Stent Siegmund; James D. Watson (1980). The double helix: a personal account of the discovery of the structure of DNA. New York: Norton. ISBN 0-393-95075-1.
- James D. Watson 2004. DNA: The Secret of Life. Random House: ISBN 978-0-09-945184-6
- Maurice Wilkins (2003). The third man of the double helix the autobiography of Maurice Wilkins. Cambridge, Eng: University Press. ISBN 0-19-860665-6.
- Russell, Peter (2001). iGenetics. New York: Benjamin Cummings. ISBN 0-8053-4553-1.
- Brown T.A. (2006). Genomes (3rd ed. izd.). Garland Science. ISBN 0815341385.
- Saenger Wolfram (1984). Principles of Nucleic Acid Structure. New York: Springer-Verlag. ISBN 0-387-90762-9.
- Butler John M. (2001). Forensic DNA Typing. Elsevier. str. 14-15. ISBN 978-0-12-147951-0. OCLC 45406517 223032110 45406517.
- Youngson (2006). Collins Dictionary of Human Biology. Glasgow: HarperCollins. ISBN 0-00-722134-7.
- Farkas, Daniel (1996). DNA simplified: the hitchhiker's guide to DNA. Washington, D.C: AACC Press. ISBN 0-915274-84-1.
- Donald Voet et al.: Lehrbuch der Biochemie. Wiley-VCH, 2002, ISBN 3-527-30519-X
- Jeremy M. Berg, Lubert Stryer et al.: Biochemie. 5. Auflage. Spektrum Akademischer Verlag, 2003, ISBN 3-8274-1303-6, Online Version, Volltextsuche
- Manfred Schartl, Manfred Gessler, Arnold von Eckardstein: Biochemie und Molekularbiologie des Menschen. 1. Auflage. Elsevier: München 2009. ISBN 978-3-437-43690-1
- Philipp Christen, Rolf Jaussi: Biochemie. Eine Einführung mit 40 Lerneinheiten. Springer-Verlag, 2005, ISBN 3-540-21164-0
- Florian Horn et al.: Biochemie des Menschen – Das Lehrbuch für das Medizinstudium. 3., vollst. überarb. u. erw. Aufl. Thieme, Stuttgart, 2005, ISBN 3-13-130883-4
- Joachim Rassow, Karin Hauser, Roland Netzker, Rainer Deutzmann: Biochemie. Georg Thieme Verlag, 2006, ISBN 3-13-125351-7
- David L. Nelson & Michael M. Cox: Lehninger Biochemie. Springer, 4. vollständig überarbeitete & erweiterte Auflage, korrigierter Nachdruck 2011. [Übersetzung der 5. amerikanischen Auflage]. ISBN 978-3-540-68637-8
- David L. Nelson & Michael M. Cox: Lehninger Principles of Biochemistry. W. H. Freeman, 6th International Edition 2013. ISBN 978-1-4641-0962-1
- Peter C. Heinrich et al.: Löffler/Petrides: Biochemie und Pathobiochemie. Springer, 9. vollständig überarbeitete Auflage 2014. ISBN 978-3-642-17971-6 (Print); ISBN 978-3-642-17972-3 (eBook)
- Paul Walden: Geschichte der organischen Chemie seit 1880, Springer-Verlag, Berlin*Heidelberg*New York 1972, ISBN 3-540-05267-4
- Peter Reuter: Taschenwörterbuch der Biochemie. Deutsch - Englisch/Englisch - Deutsch, Birkhäuser Verlag, Basel/Boston/Berlin 2000, ISBN 3-7643-6197-2
- Online-Grundkurs Arhivirano 2015-03-21 na Wayback Machine-u
- Online Biochemie Vorlesungen Arhivirano 2016-03-04 na Wayback Machine-u
- Biochemistry Online – An Approach Based on Chemical Logic – didaktisch hervorragendes Online-Lehrbuch
- Michael W. King: King's Biochemistry
- Марри Р. и др. Биохимия человека. — М., 1993.
- Введение в биохимическую экологию. — М.: Издательство Московского университета, 1986.
- Vasudevan, D. M. et al. (2013). Textbook of Biochemistry for Medical Students. JP Medical Publishers. ISBN 978-9-3509-0530-2.
- Collier, Leslie; Balows, Albert; Sussman, Max. (1998). Mahy, Brian and Collier, Leslie. Arnold. ur. Topley and Wilson’s Microbiology and Microbial Infections. Virology. ISBN 0-340-66316-2.
- Северин, Е.С. (2003). Под ред. Е.С. Северина. ur. Биохимия: Учеб. для вузов. ГЭОТАР Медиа. ISBN 5-9231-0254-4.
- Березов Т. Т., Коровкин Б. Ф. (1998). Биологическая химия: Учебник. М.: Медицина. ISBN 5-225-02709-1.
Spoljašnje veze[uredi | uredi kod]
- Virtuelna biblioteka Biohemije
- Američko hemijsko društvo
- Evropsko Društvo Biohemičara[mrtav link]
- Biochemistry, 5th ed. Full text of Berg, Tymoczko, and Stryer, courtesy of NCBI.
- Biochemistry, 2nd ed. Arhivirano 2008-07-05 na Wayback Machine-u Full text of Garrett and Grisham.
- Biochemistry Animation Arhivirano 2012-06-24 na Wayback Machine-u (Narrated Flash animations.)
- SystemsX.ch - The Swiss Initiative in Systems Biology
- Biochemistry Online Resources – Lists of Biochemistry departments, websites, journals, books and reviews, employment opportunities and events.
- Full text of Biochemistry Arhivirano 2015-07-18 na Wayback Machine-u by Kevin and Indira, an introductory biochemistry textbook.
- GBM - Gesellschaft für Biochemie und Molekularbiologie e.V.
- Möglichkeiten für ein Biochemie-Studium und verwandte Studiengänge in Deutschland
- Ringvorlesung Biochemie Arhivirano 2014-04-26 na Wayback Machine-u Videoaufzeichnungen einer Ringvorlesung zur Biochemie. Von TIMMS, Tübinger Internet Multimedia Server der Eberhard Karls Universität Tübingen.
Biohemijski naučni časopisi[uredi | uredi kod]
- The Journal of Biological Chemistry - JBC Zeitschrift der amerikanischen Gesellschaft für Biochemie und Molekularbiologie ISSN 0021-9258
- Biochemistry ISSN 0006-2960
- Biochemical Journal ISSN 0306-3275
- Chemistry and Biology ISSN 1074-5521
- Biological Chemistry ISSN 1431-6730
- FEBS Letters Arhivirano 2015-04-09 na Wayback Machine-u ISSN 0014-5793
- Biochimica et Biophysica Acta ISSN 0006-3002






