Zakon održanja mase
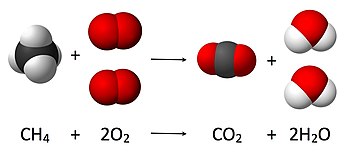
Zakon održanja mase (ili zakon očuvanja mase) predstavlja eksperimentalno utvrđenu činjenicu da je u hemijskim reakcijama masa reaktanata jednaka masi proizvoda reakcije. S obzirom na to da u nuklearnim reakcijama i pri velikim brzinama (uporedivim sa brzinom svetlosti) dolazi do pretvaranja mase u energiju ili obrnuto, može se smatrati specijalnim slučajem zakona o održanju materije.
Površnim posmatranjem nekih procesa u prirodi (kao što su rast drveta, sagorevanje sveće ili isparavanje vode) može se doći do ubeđenja da materija može nastati i nestati. Međutim pažljivim posmartanjem može se utvrditi da ovo nije slučaj. Materija može da promeni svoj oblik, agregatno stanje i sl. ali ne može nastati ni iz čega ili nestati.
Ovaj zakon se ponekada i naziva zakon o neuništivosti materije, koji glasi: Materija se ne može uništiti, niti ni iz čega stvoriti, ona može samo da se menja i da prelazi iz jednog u drugi oblik.
Zakon neuništivosti materije se izražava jednadžbom kontinuiteta.
Zakon održanja materije, jedan od najstarijih zakona fizike, formulisan je još u antičkoj Grčkoj, ali bez eksperimentalne potvrde.
A. L. Lavoazije (Lavoisier) je 1774. u eksperimentu u kome je zagrevao kalaj sa vazduhom u zatvorenom sudu primetio da je težina celog sistema ista pre i posle hemijske reakcije. Ovaj eksperiment je ukazao na činjenicu da nema pre i posle reakcije nema promene količine materije. Na osnovu svojih pokusa, Lavoazije je formulirao Zakon o održanju mase na sledeći način:
- Nikakve se promjene ne mogu opaziti u ukupnoj masi svih tvari koje sudjeluju u kemijskoj reakciji..
Na primjer, reakcija vodika s kisikom i nastanak vode:
Rezultat:
Kako je Lomonosov formulisao sličnu pravilnost nešto ranije (1748. ili 1756), zakon se ponekad zove i Lavoazje-Lomonosovljev zakon.
Ovaj zakon može se definisati:
Ukupna masa supstanci koje ulaze u reakciju jednaka je ukupnoj masi proizvoda reakcije. Ako A i B predstavljaju mase dveju supstanci koje učestvuju u nekoj hemijskoj reakciji pri kojoj nastaju mase C i D drugih dveju (hemijski promenjenih) supstanci, zakon o održanju mase se može izraziti kao:
A+B = C+D
H. Landolt (1893) i A. Heydweiller (1901) su izvršili eksperimente da bi potvrdili tačnost ovog zakona. Hans Landolt (1831.-1910.), švicarski fizički kemičar, vrlo je preciznim mjerenjima potvrdio taj zakon s točnošću 1: 107.
J. J. Maley je 1912. godine upotrebio vagu koja je bila znatno usavršena da bi se otklonio nedostatak gore navedenih eksperimenata. On je uspeo da dokaže da u slučaju reakcije između barijumhlorida i natrijumsulfata, svaka promena u masi mora biti manja od jednog milionitog dela.
Prema Einsteinovoj teoriji relativnosti, materija (kao oblik energije) i energija mogu prelaziti jedna u drugu, u međusobnom odnosu koji je definisan poznatom Ajnštajnovom jednačinom:
- E = mc2
Drugim rečima, umesto dva fundimentalna zakona: zakona o održanju mase i zakona o držanju energije, postoji samo jedan princip. Međutim, pri bilo kojoj hemijskoj promeni praćenoj promenom temperature, desiće se i odgovarajuća promena mase. Po Ajnštajnovoj formuli, mora se dio ukupne mase (m) reaktanata pretvoriti u energiju (E) kemijske reakcije prema relaciji: E = mc2, gdje je c brzina svjetlosti (2,997925• 108ms -1). Odatle slijedi da bi točnost vaganja morala biti najmanje 1:1010 da bi se ustanovio gubitak mase.




