Čvrsto agregatno stanje


Čvrsto agregatno stanje (također i kruto ili solidno) predstavlja jedno od četiri agregatna stanja materije, a prepoznatljivo je po svojstvima opiranja promenama oblika i zapremine. Najviši oblik organizacije supstance zastupljen je u čvrstom agregatnom stanju. Mnoge supstance u prirodi se nalaze upravo u ovakvom obliku organizacije. Uređenost strukturnih jedinica (atomi, molekule, ioni) u čvrstoj supstanci je znatno veća nego u tečnostima. Promjena položaja strukturnih jedinica nije moguća i one miruju, ako se zanemare oscilacije ovih strukturnih jedinica oko ravnotežnog položaja. Zbog toga čvrste supstance imaju svoju vlastitu zapreminu i vlastiti oblik. Čvrsto agregatno stanje je karakteristično po svojoj krutosti i otpornosti na promene oblika i zapremine. Za razliku od tečnosti, čvrsti objekat ne može da teče i zauzima oblik suda, niti se širi da popuni celokupnu dostupnu zapreminu kao što je to slučaj sa gasovima.
Grana fizike koja se bavi proučavanjem čvrstih supstanci je fizika čvrstog stanja, i ona je glavna grana fizike kondenzovanog stanja (koja takođe obuhvata tečnosti). Čvrste supstance se proučavaju i u sklopu nauke o materijalima, koja se prventveno bave fizičkim i hemijskim svojstvima čvrste materije. Hemija čvrstog stanja ima poseban naglasak na sintezi novih materijala, kao i na njihovoj identifikaciji i hemijskoj kompoziciji.
Vrste čvrstog agregatnog stanja[uredi | uredi kod]
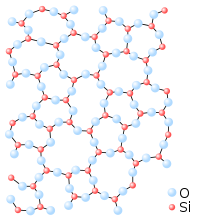
Tijela u čvrstom stanju mogu biti kristalna i amorfna. U kristalnim telima atomi su pravilno raspoređeni u prostoru i samo osciliraju oko ravnotežnih položaja. U amorfnim telima čestice isto osciluju oko ravnotežnih položaja, ali je njihov prostorni raspored neuređen.
- Kristali – ukoliko su strukturne jedinice u čvrstoj supstanci pravilno raspoređene u bilo kojem delu ili pravcu u supstanci, onda su te supstance kristali.
- Amorfno stanje – ukoliko je razmeštaj strukturnih jedinica promenjiv i različit u različitim delovima supstance, onda su to amorfne supstance. Amorfno stanje je slično tečnom agregatnom stanju i izgleda kao nagla zaleđenost strukturnih jedinica u tečnom stanju i sva neuređenost, karakteristična za tečnosti, ostala je fiksirana. Zbog toga se amorfno stanje može i zove pothlađena tečnost. Podizanjem temperature, neuređenost se postepeno povećava, približava tečnom stanju i to se manifestira kao omekšavanje. Zbog toga amorfne supstance nemaju fiksnu temperaturu topljenja, nego temperaturni interval omekšavanja. Staklo je najuobičajeni oblik amorfnog stanja.
Mikroskopski opis[uredi | uredi kod]

Atomi, molekuli ili joni koji sačinjavaju čvrstu materiju mogu da budu organizovani na uređen ponavljajući način, ili iregularno. Materijali čiji konstituenti su aranžirani u regularne paterne su poznati kao kristali. U nekim slučajevima, regularno uređenje može da bude konstantno na velikoj skali, na primer dijamanti, pri čemu je svaki dijamant jedan kristal. Čvrsti objekti koji su dovoljno veliki da se mogu videti i obrađivati su rekto sastavljeni od jednog kristala, već se umesto toga sastoje od brojnih manjih kristala, poznatih kao kristaliti. Njihova veličina može da varira od nekoliko nanometara do nekoliko metara. Takvi materijali se nazivaju polikristalnim. Skoro svi obični metali, i mnoge keramike, su polikristalni.
U drugim materijalima, ne postoji dalekosežna uređenost pozicija atoma. Takve čvrste materije su poznate kao amorfne čvrste materije; primeri su polistiren i staklo.
Da li je čvrsta materija kristalna ili amorfna zavisi od datog materijala, i uslova pod kojima je formirana. Čvrste materije koje su formirane sporim hlađenjem su uglavnom kristalne, dok čvrste materije koje su brzo očvrsnute imaju veliku verovatnoću poprimanja amorne forme. Slično tome, izbor specifične kristalne strukture formirane u kristalnoj čvrstoj materiji zavisi od datog materijala i načina na koji je čvrsto stanje formirano.
Dok mnogi objekti u širokoj upotrebi, kao što su kocke leda i metalni novac, imaju identičnu hemijsku strukturu, mnogi drugi materijali se sastoje od znatnog broja različitih supstanci upakovanih zajedno. Na primer, tipična stena je agregat nekoliko različitih minerala i mineraloida, bez specifične hemijske kompozicije. Drvo je prirodni organski materijal koji se prvenstveno sastoji od celuloznih vlakana ugrađenih u matricu organskog lignina. U nauci o materijalima, kompoziti sa više od jednog konstituentnog materijala mogu da budu dizajnirani tako da imaju željena svojstva.
Klase čvrste materije[uredi | uredi kod]
| Za više informacija pogledajte članak Vezivanje u čvrstoj materiji |
Sile između atoma u čvrstoj materiji mogu da imaju više formi. Na primer, kristal natrijum hlorida (obične soli) se sastoji od jonskog natrijuma i hlora, koji su vezani jonskim vezama. U dijamantu ili silicijumu, atomi dele elektrone i formiraju kovalentne veze. U metalima, elektroni se dele putem metalnih veza. Neke čvrste materije, a posebno organska jedinjenja, su vezana van der Valsovim silama koje proizilaze iz polarizacije oblaka elektronskih naelektrisanja molekula. Razlike među tipovima čvrstih materijala proizilaze iz razlika u njihovom vezivanju.
Metali[uredi | uredi kod]

Metali su tipično jaki, gusti, i dobro provode elektricitet i toplotu. Većina elemenata u periodnom sistemu, od onih levo od dijagonale pobučene od bora do polonijuma, su metali. Smeše dva ili više elemenata u kojim je glavna komponenta metal su poznate kao legure.
Ljudi su koristili metale u mnoge svrhe od prehistorijskih vremena. Jačina i pouzdanost metala su doveli do njihove široke rasprostranjene uloge u građevinarstvu zgrada i drugih struktura, kao i u većini vozila, mnogim uređajima i alatima, cevima, putnim znacima i železničkim šinama. Gvožđe i aluminijum su dva najčešće korišćena strukturna metala, i oni su isto tako najzastupljeniji metali u Zemljinoj kori. Gvožđe je u širokoj upotrebi u obliku legura, čelika, koji sadrži do 2,1% ugljenika, što ga čini tvrđim od čistog gvožđa.
Pošto su metali dobri provodnici elektriciteta, oni su korisni u električnim uređajima i za prenos električne sttuje preko velikih rastojanja sa malim gubitkom energije ili disipacijom. Stoga su električne mreže zavisne od metalni kablova za distribuciju elektriciteta. Kućni električni sistemi, na primer, sadrže bakar zbog njegovih dobrih provodnih svojstava i lake obradivosti. Visoka termalna provodnost većine metala ih isto tako čini koristnim za izradu kuhinjskog posuđa.
Izučavanje metallnih elemenata i njihovih legura sačinjava znatnu porciju polja hemije čvrstog stanja, fizike, nauke o materijalima i inženjerstva.
Metalne čvrste materije su vezane delokalizovanim elektronima visoke gustine, što je poznato kao „metalno vezivanje“. U metalu, atomi brzo gube svoje spoljašnje (valentne) elektrone, formirajući pozitivne jone. Slobodni elektroni su rašireni u celokupnom čvrstom materijalu, koji se održava dejstvom elektrostatičkih interakcija između jona i elektronskih oblaka.[1] Veliki broj slobodnih elektrona daje metalima njihove visoke vrednosti električne i termalne provodnosti. Slobodni elektroni takođe sprečavaju transmisiju vidljive svetlosti, te su metali neprozirni i sjajni.
Napredniji modeli metalnih svojstava razmatraju efekat pozitivnih jonskih jezgara na delokalizaciju elektrona. Većina metala ima kristalne strukture, čiji joni su obično aranžirani u obliku periodične rešetke. Matematički, potencijal jonskih jezgara se može tretirati raznim modelima, najjednostavniji od kojih je model skoro slobodnih elektrona.
Minerali[uredi | uredi kod]

Minerali su prirodne čvrste materije koje su formirane putem raznih geoloških procesa pod visokim pritiskom. Da bi bila klasifikovana kao mineral, supstanca mora da ima kristalnu strukturu sa uniformnim fizičim svojstvima. U pogledu sastava minerali se nalaze u opsegu od čistih elemenata i jednostavnih soli do veoma kompleksnih silikata sa hiljadama poznatih formi. U kontrastu s tim, uzorci stena su randomni agregati minerala i/ili mineraloida, i nemaju specifični hemijski sastav. Velika većina stena Zemljine kore se sastoji od kvarca (kristalnog SiO2), feldspata, liskuna, hlorita, kaolinita, kalcita, epidota, olivina, augita, rogovače, magnetita, hematita, limonita i nekoliko drugih minerala. Neki minerali, kao što su kvarc, liskun ili feldspat su rasprotranjeni, dok se drugi nalaze samo na nekoliko lokacija u svetu. Daleko najvaće grupa minerala su silikati (većina stena su ≥95% silikati), koji se uglavnom sastoje od silicijuma i kiseonika, sa dodatkom jona aluminijuma, magnezijuma, gvožđa, kalcijuma i drugih metala.
Keramika[uredi | uredi kod]

Keramika se sastoji od neorganskih jedinjenja, obično oksida hemijskih elemenata. Oni su hemijski inertni, i često su otporni na hemijsku eroziju do koje dolazi u kiseloj ili kaustičnoj sredini. Keramike generalno mogu da podnesu visoke temperature u opsegu od 1000 do 1600 °C (1800 do 3000 °F). Izuzeci su neoksidni neorganski materijali, kao što su nitridi, boridi i karbidi.
Tradicionalne sirovine za izradu keramike obuhvataju glinene minerale kao što je kaolinit, dok se od nedavno koristi i aluminijum oksid (alumina). Moderni keramički materali, koji se klasifikuju kao napredne keramike, sadrže silicijum karbid i volfram karbid. Ovi materijali poseduju znatnu abrazivnu otpornost, i stoga nalaze primenu u habajućim pločama rudarske opreme za mlevenje materijala.
Većina keramičkih materijala, kao što su alumina i srodna jedinjenja, su formirani iz finih prahova, iz kojih nastaju polikristalne mikrostrukture fine granulacije, koji su bogati centrima rasipanja svetlosti čija veličina je uprediva sa talasnom dužinom vidljive svetlosti. Stoga su oni generalno neprozirni materijali, za razliku od transparentnih materijala. Nedavno razvijena nanoskalna tehnologija (e.g. sol-gel), međutim, omogućila je produkciju polikristalne transparentne keramike, kao što je transparentna alumina i jedinjenja alumine, za takve primene kao što su laseri visoke snage. Napredne keramike se takođe koriste u medicini, električnim i elektronskim industrijama.
Keramičko inženjerstvo je nauka i tehnologija pravljenja čvrstih keramičkih materijala, delova i uređaja. To se radi bilo dejstvom toplote, ili na nižim temperaturama, koristeći reakcije precipitacije iz hemijskih rastvora. Termin obuhvata prečišćavanje sirovina, izučavanje i produkciju hemijskih jedinjenja, njihovog formiranja u komponente, i izučavanje njihove strukture, sastava i svojstava.
S mehanističkog gledišta, keramički materijali su krti, tvrdi, otporni na komresiju i slabi pri smicanju i naprezanju. Krhki materijali mogu da ispolje znatnu vlačnu čvrstoću pri podržavanju statičkog tereta. Žilavost pokazuje koliko energije materijal može da apsorbuje pre mehaničkog neuspeha, dok žilavost loma (označena sa KIc ) opisuje sposobnost materijala sa naslednim mikrostrukturnim defektima da se odupre lomu u obliku rasta i propagacije rascepa. Ako material ima veliku vrednost žilavosti loma, bazni principi mehanike loma sugerišu da će on verovatno doživiti prelom pri istezanju. Krti prelom je karakterističan za većinu keramičkih i stakleno-keramičkih materijala koji tipično ispoljavaju niske (i inkonzistentne) vrednosti KIc.
Primer upotrebe keramike ekstremne tvrdoće od Zirkonijuma je primena u proizvodnji oštrica noževa, kao i drugih industrijskih alata za sečenje. Keramike kao što su alumina, bor karbid i silicijum karbid su korišćene u pancirnim prslucima za odbijanje metaka iz puški velikog kalibra. Silicijum nitridni delovi se koriste u keramičkim ležajevima, gde ih njihova tvrdoća čini otpornim na habanje. Keramika je isto tako hemijski otporna i može se koristiti u vlažnim okruženjima, gde bi čelični ležajevi bili podložni oksidaciji (ili rđanju).
Još jedan primer primene keramike je adiabatski keramički motor sa operativnom temperaturom od preko 6000 °F (3300 °C) koji je razvila Toyota tokom ranih 1980-tih. Keramički motorima nisu potrebni sistemi za hlađenje, što omogućava znatnu redukciju težine i stoga efikasniju upotrebu goriva. U konvencionalnim metalnim motorima, znatan deo energije oslobođene iz goriva se gubi u obliku otpadne toplote da bi se sprečilo topljenje metalnih delova. Takođe se radi na razvoju keramičkih delova za gasno turbinske motore. Turbinske mašine od keramike mogu da efiktivnije rade, što daje avionu veži opseg leta i nosivost za datu količinu goriva. Međutim, takve mašine nisu u proizvodnji zato što je proizvodnja keramičkih delova sa dovoljnom preciznošću i trajnošću teška i skupa. Metode obrade često proizvode široku distribuciju mikroskopskih mana koje frekventno imaju detrimentalnu ulogu u procesu sinteriranja, što dovodi do proliferacije pukotina, i ultimativno mehaničkog kvara.
Staklena keramika[uredi | uredi kod]

Stakleno-keramički materijali imaju mnoštvo zajedničkih svojstava sa nekristalnim staklima i kristalnim keramikama. Oni se formiraju kao staklo, i zatim se parcijalno kristalizuju toplotnim tretmanom, proizvodeći amorfne i kristalne faze tako da su kristalna zrna ugrađena u nekristalnu intergranularnu fazu.
Stakleno-keramika se koristi za pravljenje posuđa za kuvanje (originalno poznatog pod imenom CorningWare) i ploča šporeta, koji imaju visoku otpornost na termalni šok i ekstremno nisku permeabilnost za tečnosti. Negativni koeficijenat termičke ekspanzije kristalne keramičke faze može da bude balansiran pozitivnim koeficijentom staklene faze. Na oređenoj tački (~70% kristalnoj) tečna-keramika ima neto koeficijenat termičke ekspanzije blizak nuli. Taj tip staklene-keramike manifestuje izuzetna mehanička svojstva i može da izdrži ponovljene i brze temperaturne promene do 1000 °C.
Staklena-keramika se može isto tako prirodno formirati kad grom udari u kristalna (e.g. kvarcna) zrna prisutna na većini peščanih plaža. U tom slučaju, ekstremna i brza toplota groma (~2500 °C) kreira šuplju, razgranatu poput korena, strukturu koja se naziva fulgurit putem topljenja.
Organske čvrste materije[uredi | uredi kod]
Organska hemija izučava strukture, svojstva, sastav, reakcije, i sintetičku pripremu hemijskih jedinjenja ugljenika i vodonika, koja mogu da sadrže niz drugih elemenata, kao što su azot, kiseonik i halogeni: fluor, hlor, brom i jod. Neka organska jedinjenja takođe mogu da sadrže elemente fosfor ili sumpor. Primeri organskih čvrstih materijala obuhvataju drvo, parafinski vosak, naftalen i široki opseg polimera i plastika.
Drvo[uredi | uredi kod]
Drvo je prirodni organski materijal koji se prvenstveno sastoji od celuloznih vlakana ugrađenih u ligninsku matricu. U polgedu mehaničkih svojstava, vlakna su jaka pri naprezanju, a ligninska osnova je otporna na kompresiju. Stoga je drvo bilo jedan od važnih građevinskih materijala još od početka ljudske izgradnje skloništa i korišćenja brodova. Drvo koje se koristi za građevinski rad je poznato kao drvena građa. U građevinarstvu, drvo nije samo strukturni materijal, nego se koristi i za formiranje šalunga za beton.
Na drvetu bazirani materijali se takođe ekstenzivno koriste za pakovanje (e.g. karton) i papir, koji se prave od rafinirane pulpe. Hemijski pulpni procesi koriste kombinaciju visoke temperature i alkalnih (kraft) ili kiselih (sulfit) hemikalija za razlaganje hemijskih veza lignina.
Polimeri[uredi | uredi kod]

Jedno važno svojstvo ugljenika u organskoj hemiji je da može da formira izvesna jedinjenja, čiji pojedinačni molekuli imaju sposobnost vezivanja jedan za drugi, čime se formiraju lanci ili mreže. Proces se naziva polimerizacijom, a lanci ili mreže polimerima, dok su izvorna jedinjenja monomeri. Postoje dve glavne grupe polimera: oni koji su veštački napravljeni se nazivaju industrijskim polimerima ili sintetičkim polimerima (plastikama) i oni koji se javljaju u prirodi kao biopolimeri.
Monomeri mogu da imaju razne hemijske substituente, ili funkcionalne grupe, što može da utiče na hemijska svojstva organskih jedinjenja, kao što su rastvorljivost i hemijska reaktivnost, kao i na fizička svojstva, kao što su tvrdoća, gustina, mehanička ili zatezna jačina, otpornost na habanje, toplotna otpornost, transparencija, boja, etc.. U proteinima, te razlike daju polimeru sposobnost da poprimi biološki aktivnu konformaciju.

Ljudi su koristili prirodne organske polimere vekovima u obliku voskova i šelaka, koji se klasifikuju kao termoplastični polimeri. Biljni polimer pod imenom celuloza pruža zateznu čvstoću prirodnim vlaknima i kanapima, a do ranog 19. veka prirodne gume su ušle u široku upotrebu. Polimeri su sirovine (rezini) koje se koriste za pravljenje plastike. Plastika je finalni proizvod, kreiran nakon što se jedan ili više polimera ili aditiva doda rezinu tokom presovanja, i smeša se oblikuje u finalnu formu. Polimeri koji su dostupni i u širokoj upotrebi obuhvataju na ugljeniku bazirane: polietilen, polipropilen, polivinil hlorid, polistiren, najlone, poliester, akrilne rezine, poliuretan, i polikarbonate, i na silicijumu bazirane silikone. Plastike se generalno klasifikuju kao roba, specijalizovani proizvodi i inženjerske plastike.
Kompozitni materijali[uredi | uredi kod]


Kompozitni materijali sadrže dve ili više makroskopske faze, jedna od koji je obično keramička. Na primer, kontinuirana matrica, i dispergovana faza keramičkih čestica ili vlakana.
Primene kompozitnih materijala su u opsegu od strukturnih elemenata kao što je čelikom ojačani beton, do termičkih izolacionih pločica koje igraju ključnu ulogu u termalnoj zaštiti Spejs šatla. Jedan primer je ojačani ugljenik-ugljenik (engl. Reinforced Carbon-Carbon - RCC), lagani sivi materijal koji može da podnese temperature povratka u atmosferu do 1510 °C (2750 °F) i da zaštiti nos i vodeće ivice krila letilice. RCC je laminirani kompozitni materijal izrađen od grafitne rejonske tkanine i impregniran sa fenolnim rezinom. Nakon stvrdnjavanja na visokim temperaturama u autoklavu, dolazi do pirolize laminata i prelaza iz rezina u ugljenik, impregniran sa furfuralnim alkoholom u vakumnoj komori. Stvrdnjavanje/piroliza konvertuje furfural alkohol u ugljenik. Da bi se pružila oksidaciona otpornost radi višestruke upotrebe, spoljašnji slojvi RCC-a se konvertuju u silicijum-karbid.
Primer kompozitnog materijala iz domaćinstva se može videti u „plastičnim“ kućištima televizijskih aparata, celularnih telefona itd. Ta plastična kućišta se obično sastoje od kompozita napravljenog od termoplastične matrice sa akrilonitril butadien stirenom (ABS) pri čemu su kalcijum karbonatna kreda, talk, staklena vlakna ili ugljena vlakna dodata radi ojačanja, mase, ili elektro-statičke disperzije. Ti dodaci se mogu nazivati ojačavajućim vlaknima, ili disperzantima, u zavisnosti od svrhe.
Stoga, materijal matrice okružuje i pojačava materijal ojačanja održavajući njihove relativne pozicije. Ojačanja utiču na mehanička i fizička svojstva matrice. Sinergizam proizvodi osobine materijala koje individualni konstituenti nemaju, dok veliki broj različitih matrica i ojačavajućih materijala pruža izvor dezajneru da ostvari optimalnu kombinaciju.
Poluprovodnici[uredi | uredi kod]

Poluprovodnici su materijali čija električna otpornosti (i provodnost) je između metalnih provodnika i nemetalnih izolatora. Oni se nalaze u periodnoj tabeli idući dijagonalno na dole i desno polazeći od bora. Oni razdvajaju električne provodnike (ili metale, na levoj strani) i izolatore (na desnoj strani).
Uređaji napravljeni od poluprovodnih materijala su u osnovi moderne elektronike, uključujući radio, računare, telefone, etc. Poluprovodnički uređaji obuhvataju tranzistore, solarne ćelije, diodes i integralna kola. Solarni fotovoltni paneli su veliki poluprovodnički uređaji koji direktno konvertuju svetlo u električnu energiju.
U metalnim provodnicima, struja se prenosi protokom elektrona, dok se u poluprovodnicima struja prenosi bilo elektronima ili pozitivno naelektrisanim „rupama“ u elektronskoj strukturi materijala. Poluprovodnički materijali u širokoj upotrebi su silicijum, germanijum i galijum arsenid.
Nanomaterijali[uredi | uredi kod]
Mnoge tradicionalne čvrste materije ispoljavaju različita svojstva kad se dovedu do nanometarske veličine. Na primer, nanočestice obično žutog zlata i sivog silicijuma imaju crvenu boju; nanočestice zlata se tope na znatno nižim temperaturama (~300 °C pri veličini od 2,5 nm) od zlatnih ploče (1064 °C);[2] i metalne nanožice su znatno jače od korespondirajuće veće mase matala.[3][4] Velika površina nanočestica ih čini ekstremno privlačnim za pojedine primene u polju energetike. Na primer, platina može da služi kao katalizator za automobilsko gorivo, kao i membrana protonske razmene (PEM) gorivih čelija. Keramički oksidi (ili kermeti) lantana, cerijuma, mangana i nikla se izučavaju za moguću primenu u čvrstim oksidnim gorivim ćelijama (SOFC). Litijum, litijum–titanatne i tantalne nanočestice se koriste u litijumskim jonskim baterijama. Silicijumske nanočestice mogu da dramatično povećaju skladišni kapacitet litijumskih jonskih baterija tokom ciklusa ekspanzije/kontrakcije. Silicijumske nonočestice funkcionišu bez znatne degradacije i potencijalno mogu da nađu primenu u u baterijama sa znatno povećanim kapacitetom. Silicijumske nanočestice se takođe koriste u novim formama ćelija za dobijanje solarne energije. Depozicija tankih filmova silicijumskih kvantnih tački na polikristalne silicijumske supstrate fotovoltnih (solarnih) ćelija povećava naponski izlaz za 60% putem fluorescencije ulaznog svetla pre transformacije u električnu energiju. Ovde isto tako, površina nanočestica (i tankih filmova) igra kritičnu ulogu u maksimizaciji količine apsorbovane radijacije.
Fizička svojstva[uredi | uredi kod]
Fizička svojstva elemenata i jedinjenja koja pružaju uvedljivu evidenciju o hemijskom sastavu obuhvataju miris, boju, zapreminu, gustinu (masu po jedinici zapremine), tačku topljenja, tačku ključanja, toplotni kapacitet, fizičku formu i oblik na sobnoj temperaturi (čvrsta materija, tečnost ili gas; kubni, trigonalni kristali, etc.), tvrdoću, poroznost, indeks refrakcije i mnoga druga. Ova sekcija diskutuje neka od fizičkih svojstava materijala u čvrstom stanju.
Mehanička svojstva[uredi | uredi kod]
Mehanička svojstva materijala opisuju karakteristike kao što je jačina ili otpornost na deformaciju. Na primer, čelični stubovi se koriste u građevini zbog njihove velike jačine, što znači da se oni ne lome niti se znatno savijaju pod teretom.
Mehanička svojstva obuhvataju: elastičnost i plastičnost, zateznu čvrstoću, kompresivnu jačinu, otpornost na smicanje, otpornost na lomljenje, duktilnost (koja je niska kod lomljivih materijala), i tvrdoću zasecanja. Mehanika čvrstog stanja je izučavanje ponašanja čvrstog materijala pod spoljašnjim uticajima kao što su spoljašnje sile i promene temperature.
Čvrsti materijali ne manifestuju makroskopski protok, za razliku od fluida. Svako odstupanje od njihovog originalnog oblika se naziva deformacijom. Proporcija deformacija i originalne veličine se naziva naprezanjem. Ako je primenjeni stres dovoljno nizak, skoro svi čvrsti materijali se ponašaju na takav način da je naprezanje direktno proporcionalno stresu (Hukov zakon). Koeficijent proporcije se naziva modul elastičnosti ili Jangov modul. Region deformacije je poznat kao linearno elastični region. Tri modela mogu da opišu način na koji čvrsti materijali odgovaraju na primenjeni stres:
- Elastičnost – Kad se primenjeni stres ukloni, materijal se vraća u svoje nedeformisano stanja.
- Viskoelastičnost – Ovi materijali se ponašaju elastično, ali takođe imaju prigušivanje. Kad se primenjeni stres ukloni, neophodno je uložiti rad protiv efekta prigušivanja i dolazi do konvertovanja rada u toplotu u materijalu. To dovodi do histerezisne petlje u krivi stresa–naprezanja. Iz ovog sledi da je mehanički rad vremenski zavistan.
- Plastičnost – Materijali koji su elastični generalno zadržavaju to svojstvo dok je primenjeni stres manji od vrednosti popuštanja. Kad stres premaši vrednost popuštanja, materijal se ponaša plastično i ne vraća se u prethodno stanje. Dolazi do ireverzibilne plastične deformacije (ili viskoznog protoka) nakon popuštanja, što je permanentno.
Termalna svojstva[uredi | uredi kod]

Pošto čvrste materije imaju termalnu energiju, njihovi atomi vibriraju oko fiksnih srednjih pozicija unutar uređene (ili neuređene) rešetke. Spektar vibracija rešetke u kristalnim i staklastim mrežama je u osnovi kinetičke teorije čvrstog stanja. To kretanje se javlja na atomskom nivou, i stoga se ne može opaziti ili detektovati bez visoko specijalizovane opreme, kao što je spektroskopska oprema.
Termalna svojstva čvrste materije obuhvataju termalnu provodnost, koja je svojstvo materijala da provodi toplotu. Čvrste materije takođe imaju specifični toplotni kapacitet, koji je sposobnost materijala da prima i zadržava energiju u obliku toplote (ili termalnih vibracija rešetke).
Električna svojstva[uredi | uredi kod]
Električna svojstva obuhvataju provodnost, otpornost, impedansu i kapacitancu. Električni provodnici kao što su metali i legure stoje u kontrastu sa električnim izolatorima kao što su stakla i keramike. Poluprovodnici su negde u sredini. Dok je provodnost u metalima uzrokovana elektronima, elektroni i pozitivne šupljine doprinose struju kod poluprovodnika. Alternativno, joni prenose električnu struju u jonskim provodnicima.
Mnogi materijali takođe manifestuju superprovodnost na niskim temperaturama; oni obuhvataju metalne elemente kao što su kalaj i aluminijum, razne metalne legure, neke jako dopirane poluprovodnike, i pojedine keramike. Električna otpornost većine električnih (metalnih) provodnika generalno postepeno opada sa sniženjem temperature, mada ostaje konačna. I superprovodnicima međutim, otpornost naglo pada na nulu kad se materijal ohladi ispod svoje kritične temperature. Električna struja u superprovodničkoj petlji se može beskonačno održati bez izvora energije.
Dielektrik, ili električni izolator, je supstanca koja je visoko otporna na protok električne struje. Dielektrik, kao što je plastika, ima tendenciju koncentrovanja primenjenog električnog polja unutar sebe, što je svojsto koje nalazi primenu u kondenzatorima. Kondenzator je električni uređaj koji može da uskladišti energiju u električnom polju između para provodnika na malom rastojanju ('ploča'). Kada se primeni napon na kondenzator, električna naelektrisanja jednakih magnituda, ali suprotnih polarnosti, se formiraju u svakoj ploči. Kondenzatori se koriste u električnim kolima kao uređaji za čuvanje energije, kao i u elektronskim filterima za diferencijaciju između visokofrekventnih i niskofrekventnih signala.
Optička svojstva[uredi | uredi kod]
Materijali mogu da transmituju (e.g. staklo) ili reflektuju (e.g. metali) vidljivu svetlost.
Mnogi materijali prenose neke talasne dužine dok blokiraju druge. Na primer, prozorsko staklo je transparentno za vidljivu svetlost, a u znatno manjoj meri nije propustno za većinu frekvencija ultraljubičaste svetlosti, koja uzrokuje opekotine od sunca. To svojstvo se koristi za frekventno-selektivne optičke filtere, koji mogu da menjaju boju upadnog svetla.
Za neke svrhe, optička i mehanička svojstva materijala mogu da budu od interesa. Na primer, senzori u raketama sa infracrvenim navođenjem (traženjem toplote) moraju da budu zaštićeni pokrivačem koji je transparentan za infracrvenu radijaciju. Sadašnji materijal izbora za rakete velike brzine vođene infracrvenom radijacijom je jednokristalni safir. Optički prenos safira ne pokriva celokupni srednji infracrveni opseg (3–5 µm), ali počinje da opada na talasnim dužinama većim od aproksimativno 4,5 µm na sobnoj temperaturi. Dok je jačina safira bolja od drugih dostupnih materijala za središnji infracrveni opseg na sobnoj temperaturi, on slabi iznad 600 °C. Postoji dugoročni kompromis između optičke propustnosti i mehaničke izdržljivosti. Očekuje se da će novi materijali kao što je transparentna keramika ili optički nanokompoziti imati poboljšanu performancu.
Navođenim prenosom svetlosnih talasa se bavi polje optičkih vlakana. Ova tehnologija se zaniva na sposobnosti pojedinih tipova stakla da simultano prenose sa malim gubitkom intenziteta opseg frekvencija (multimodni optički talasni vodiči) sa neznatnom interferencijom između njih. Optički talasni vodiči se koriste kao komponente u integralnim optičkim kolima ili kao transmisioni medijum u optičkim komunikacionim sistemima.
Vidite još[uredi | uredi kod]
Reference[uredi | uredi kod]
- ↑ Mortimer, Charles E. (1975). Chemistry: A Conceptual Approach (3rd izd.). New York:: D. Van Nostrad Company. ISBN 0-442-25545-4.
- ↑ Buffat, Ph.; Borel, J.-P. (1976). „Size effect on the melting temperature of gold particles”. Physical Review A 13 (6): 2287. Bibcode 1976PhRvA..13.2287B. DOI:10.1103/PhysRevA.13.2287.
- ↑ Walter H. Kohl (1995). Handbook of materials and techniques for vacuum devices. Springer. str. 164–167. ISBN 1-56396-387-6.
- ↑ Shpak, Anatoly P; Kotrechko, Sergiy O; Mazilova, Tatjana I; Mikhailovskij, Igor M (2009). „Inherent tensile strength of molybdenum nanocrystals”. Science and Technology of Advanced Materials 10 (4): 045004. Bibcode 2009STAdM..10d5004S. DOI:10.1088/1468-6996/10/4/045004.