Magnezijum karbonat – razlika između verzija
Prijeđi na navigaciju
Prijeđi na pretragu
Uklonjeni sadržaj Dodani sadržaj
m + |
Nema sažetka izmjene |
||
| Red 6: | Red 6: | ||
| Name = Magnezijum karbonat |
| Name = Magnezijum karbonat |
||
| Section1 = {{Chembox Identifiers |
| Section1 = {{Chembox Identifiers |
||
| ⚫ | |||
| ⚫ | |||
| verifiedrevid = 400293819 |
|||
| ⚫ | |||
| ChemSpiderID_Ref = {{chemspidercite|correct|chemspider}} |
|||
| ⚫ | |||
| ChemSpiderID = 10563 |
|||
| ChEMBL_Ref = {{ebicite|changed|EBI}} |
|||
| ChEMBL = 1200736 |
|||
| InChI = 1/CH2O3.Mg/c2-1(3)4;/h(H2,2,3,4);/q;+2/p-2 |
|||
| InChIKey = ZLNQQNXFFQJAID-NUQVWONBAU |
|||
| ChEBI_Ref = {{ebicite|correct|EBI}} |
|||
| ChEBI = 31793 |
|||
| SMILES = [Mg+2].[O-]C([O-])=O |
|||
| StdInChI_Ref = {{stdinchicite|correct|chemspider}} |
|||
| StdInChI = 1S/CH2O3.Mg/c2-1(3)4;/h(H2,2,3,4);/q;+2/p-2 |
|||
| StdInChIKey_Ref = {{stdinchicite|correct|chemspider}} |
|||
| StdInChIKey = ZLNQQNXFFQJAID-UHFFFAOYSA-L |
|||
| ⚫ | |||
| CASNo_Ref = {{cascite|correct|CAS}} |
|||
| CASOther = <br> 13717-00-5 (monohydrate) <br> 5145-48-2 (dihydrate) <br> 14457-83-1 (trihydrate) <br> 61042-72-6 (pentahydrate) |
|||
| PubChem = 11029 |
|||
| ⚫ | |||
| ATCCode_prefix = A02 |
|||
| ATCCode_suffix = AA01 |
|||
| ATC_Supplemental = {{ATC|A06|AD01}} |
|||
}} |
}} |
||
| Section2 = {{Chembox Properties |
| Section2 = {{Chembox Properties |
||
Verzija na datum 19 april 2014 u 20:42
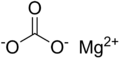
| Magnezijum karbonat | |||
|---|---|---|---|
| |||
| Drugi nazivi | Poznati su di-, tri- i penta-hidrat | ||
| Identifikacija | |||
| CAS registarski broj | 546-93-0 13717-00-5 (monohydrate) 5145-48-2 (dihydrate) 14457-83-1 (trihydrate) 61042-72-6 (pentahydrate) | ||
| PubChem[1][2] | 11029 | ||
| ChemSpider[3] | 10563 | ||
| MeSH | |||
| ChEBI | 31793 | ||
| ChEMBL[4] | CHEMBL1200736 | ||
| RTECS registarski broj toksičnosti | OM2470000 | ||
| ATC code | A02,A06AD01 | ||
| Jmol-3D slike | Slika 1 | ||
| |||
| |||
| Svojstva | |||
| Molekulska formula | MgCO3 | ||
| Molarna masa | 84.32 g/mol | ||
| Agregatno stanje | bela čvrsta supstanca | ||
| Gustina | 2.958 g/cm3, osnovno | ||
| Tačka topljenja |
350 °C razlaže se | ||
| Rastvorljivost u vodi | 10.6 mg/100 ml | ||
| Struktura | |||
| Kristalna rešetka/struktura | Romboedarska | ||
| Termohemija | |||
| Standardna entalpija stvaranja jedinjenja ΔfH |
-1111.69 kJ/mol | ||
| Standardna molarna entropija S |
65.84 J.K−1.mol−1 | ||
| Srodna jedinjenja | |||
| Drugi katjoni | Kalcijum-karbonat Stroncijum-karbonat Barijum-karbonat | ||
| Сродна једињења | artinit hidromagnezit dipingit | ||
|
| |||
| Infobox references | |||
Magnezijum karbonat, poznat i kao mineral magnezit kada je otkriven u prirodi, je hemijsko jedinjenje sa mnogo primena. Pri normalnim uslovima to je belo ili bezbojno hemijsko jedinjenje, male gustine, sa molekulskom formulom: MgCO3.[5][6] U hemiji se koristi za dobijanje magnezijum oksida, jer se na temperaturi preko 540 °C razlaže na magnezijum oksid i Ugljen dioksid. Magnezijum karbonat je magnezijumova so ugljene kiseline.
Reference
- ↑ Li Q, Cheng T, Wang Y, Bryant SH (2010). „PubChem as a public resource for drug discovery.”. Drug Discov Today 15 (23-24): 1052-7. DOI:10.1016/j.drudis.2010.10.003. PMID 20970519.
- ↑ Evan E. Bolton, Yanli Wang, Paul A. Thiessen, Stephen H. Bryant (2008). „Chapter 12 PubChem: Integrated Platform of Small Molecules and Biological Activities”. Annual Reports in Computational Chemistry 4: 217-241. DOI:10.1016/S1574-1400(08)00012-1.
- ↑ Hettne KM, Williams AJ, van Mulligen EM, Kleinjans J, Tkachenko V, Kors JA. (2010). „Automatic vs. manual curation of a multi-source chemical dictionary: the impact on text mining”. J Cheminform 2 (1): 3. DOI:10.1186/1758-2946-2-3. PMID 20331846.
- ↑ Gaulton A, Bellis LJ, Bento AP, Chambers J, Davies M, Hersey A, Light Y, McGlinchey S, Michalovich D, Al-Lazikani B, Overington JP. (2012). „ChEMBL: a large-scale bioactivity database for drug discovery”. Nucleic Acids Res 40 (Database issue): D1100-7. DOI:10.1093/nar/gkr777. PMID 21948594.
- ↑ Housecroft C. E., Sharpe A. G. (2008). Inorganic Chemistry (3rd izd.). Prentice Hall. ISBN 978-0-13-175553-6.
- ↑ Holleman A. F., Wiberg E. (2001). Inorganic Chemistry (1st edition izd.). San Diego: Academic Press. ISBN 0-12-352651-5.
