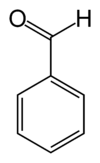
Benzaldehid
| Benzaldehid | |||
|---|---|---|---|
 |
 | ||
| Drugi nazivi | Fenilmetanal Benzenkarboksaldehid Benzoinski aldehid | ||
| Identifikacija | |||
| CAS registarski broj | 100-52-7 | ||
| PubChem[1][2] | 240 | ||
| ChemSpider[3] | 235 | ||
| UNII | TA269SD04T | ||
| EC-broj | 202-860-4 | ||
| KEGG[4] | |||
| ChEBI | 17169 | ||
| ChEMBL[5] | CHEMBL15972 | ||
| Jmol-3D slike | Slika 1 Slika 2 | ||
| |||
| |||
| Svojstva | |||
| Molekulska formula | C7H6O | ||
| Molarna masa | 106.12 g mol−1 | ||
| Agregatno stanje | bezbojna tečnost | ||
| Gustina | 1.0415 g/ml, tečnost | ||
| Tačka topljenja |
−26 °C | ||
| Tačka ključanja |
178.1 °C | ||
| Rastvorljivost u vodi | 0.6 g/100 ml (20 °C) | ||
| Viskoznost | 1.4 cP (25 °C) | ||
| Termohemija | |||
| Standardna entalpija stvaranja jedinjenja ΔfH |
−36.8 kJ/mol | ||
| Std entalpija sagorevanja ΔcH |
−3525.1 kJ/mol | ||
| Opasnost | |||
| Podaci o bezbednosti prilikom rukovanja (MSDS) | J. T. Baker | ||
| EU-klasifikacija | Štetan (Xn) | ||
| NFPA 704 | |||
| R-oznake | R22 | ||
| S-oznake | S2, S24 | ||
| Tačka paljenja | 63 °C | ||
| Srodna jedinjenja | |||
| Srodna jedinjenja | Benzil alkohol Benzojeva kiselina | ||
|
Ukoliko nije drugačije napomenuto, podaci se odnose na standardno stanje (25 °C, 100 kPa) materijala | |||
| Infobox references | |||
Benzaldehid (C6H5CHO) je organsko jedinjenje koje se sastoji od benzenskog prstena sa formil supstituentom. On je najjednostavniji aromatični aldehid i jedan od najkorisnijih u pogledu industrijske primene. Ova bezbojna tečnost ima karakterističan prijatan bademu sličan miris. Benzaldehid je primarna komponenta gorkog bademovog ulja i može se ekstrahovati iz brojnih drugih prirodnih izvora.[6]
Proizvodnja[uredi | uredi kod]
Benzaldehid se moše dobiti na više načina. Procenjuje se da je tokom 1980-thi 18 miliona kilograma proizvedeno godišnje u Japanu, Evropi, i Severnoj Americi, i očekuje se da će se taj nivo proizvodenje nastaviti. Trenutno su hlorinacija u tečnoj fazi i oksidacija toluena glavni načini dobijanja. Brojne druge metode su bile razvijene, kao što je parcijalna oksidacija benzil alkohola, alkalna hidroliza benzal hlorida, i karbonilacija benzena.[7]
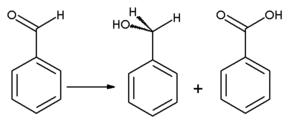
Reakcije[uredi | uredi kod]
Oksidacijom se benzaldehid konvertuje u bezmirisnu benzojevu kiselinu, koja je česta nečistoća u laboratorijskim uzorcima. Benzil alkohol se može formirati iz benzaldehida hidrogenacijom. Reakcija benzaldehida sa bezvodnim natrijum acetatom i acetatnim anhidridom proizvodi cinaminsku kiselinu, dok se alkoholni kalijum cijanid može koristiti za katalizu kondenzacije benzaldehida u benzoin. Benzaldehid podleže disproporcionaciji pri tretmanu sa koncentrovanim alkalijama (Kanizarova reakcija): jedan molekul aldehida se redukuje u korespondirajući alkohol, a drugi molekul se istovremeno oksiduje u natrijum benzoat.
Upotreba[uredi | uredi kod]
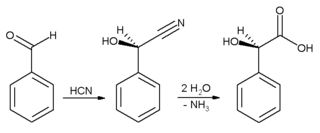
On se često koristi za davanje bademovog ukusa. Benzaldehid se koristi prvenstveno kao prekurzor za druga organska jedinjenje, od lekova do plastičnih aditiva. Anilinska boja malahitno zeleno se priprema iz benzaldehid i dimetilanilina. On je takođe prekurzor pojedinih akridinskih boja. Putem aldolne kondenzacije, benzaldehid se konvertuje u derivate cinamaldehida i stirena. Sinteza mandelinske kiseline počinje od benzaldehida:
Prvo se doda hidrocijanatna kiselina benzaldehidu, i rezultirajući nitril se naknadno hidrolizuje do mandelinske kiseline. Gornja reakcija prikazuje samo jedan od dva formirana enantiomera.
Literatura[uredi | uredi kod]
- ↑ Li Q, Cheng T, Wang Y, Bryant SH (2010). „PubChem as a public resource for drug discovery.”. Drug Discov Today 15 (23-24): 1052-7. DOI:10.1016/j.drudis.2010.10.003. PMID 20970519.
- ↑ Evan E. Bolton, Yanli Wang, Paul A. Thiessen, Stephen H. Bryant (2008). „Chapter 12 PubChem: Integrated Platform of Small Molecules and Biological Activities”. Annual Reports in Computational Chemistry 4: 217-241. DOI:10.1016/S1574-1400(08)00012-1.
- ↑ Hettne KM, Williams AJ, van Mulligen EM, Kleinjans J, Tkachenko V, Kors JA. (2010). „Automatic vs. manual curation of a multi-source chemical dictionary: the impact on text mining”. J Cheminform 2 (1): 3. DOI:10.1186/1758-2946-2-3. PMID 20331846.
- ↑ Joanne Wixon, Douglas Kell (2000). „Website Review: The Kyoto Encyclopedia of Genes and Genomes — KEGG”. Yeast 17 (1): 48–55. DOI:10.1002/(SICI)1097-0061(200004)17:1<48::AID-YEA2>3.0.CO;2-H.
- ↑ Gaulton A, Bellis LJ, Bento AP, Chambers J, Davies M, Hersey A, Light Y, McGlinchey S, Michalovich D, Al-Lazikani B, Overington JP. (2012). „ChEMBL: a large-scale bioactivity database for drug discovery”. Nucleic Acids Res 40 (Database issue): D1100-7. DOI:10.1093/nar/gkr777. PMID 21948594.
- ↑ „United States Patent 1416128 - Process of treating nut kernels to produce food ingredients.”.
- ↑ Friedrich Brühne and Elaine Wright “Benzaldehyde” in Ullmann's Encyclopedia of Industrial Chemistry, 2002, Wiley-VCH, Weinheim. DOI:10.1002/14356007.a03_463