Lewisove kiseline i baze
Luisova kiselina je od strane IUPACA definisana kao "molekularni entitet (i odgovarajuće hemijske vrste) koji je primaoc elektronskog para i zbog toga u mogućnosti da reaguje sa Luisovom bazom pri čemu se stvara zajednički adukt, tako što se dijeli elektronski par koji je dala Luisova baza". Ilustrativni primjer je reakcija između trimetilbora i amonijaka pri čemu se dobije adukt Me3BNH3.
Luisova kiselina je definisana kao bilo koja vrsta koja prihvata elektronski par. Luisova baza je bilo koja vrsta koja daje elektronski par. Zbog toga je H+ Luisova kiselina zbog toga što može prihvatiti elektronski par, a OH- i NH3 su Luisove baze zato što mogu donirati slobodan elektronski par.
Opisivanje adukata[uredi | uredi kod]
U mnogim slučajevima interakcija između bora i azota se označava sa strelicom Me3B←-NH3 pri čemu njen smjer pokazuje od Luisove baze do Luisove kiseline. Neki izvori označavaju Luisovu bazu sa parom tačaka na Luisovoj bazi kao i na aduktu, kao što je prikazano:
- Me3B + :NH3 → Me3B:NH3
U opštem slučaju veza između donora i akceptora se posmatra kao korak između kovalentne i jonske veze.
Istorijat[uredi | uredi kod]
Ovaj koncept je prvi predstavio Gilbert Njutn Luis koji je predložio teoriju hemijske veze 1923. Iste godine je bila objavljena Bronsted-Lourijeva teorija kiselina i baza. Dvije teorije su različite ali komplementarne. Luisova baza je ujedno i Bronsted-Lourijeva baza, ali Luisova kiselina ne mora biti ujedno i Bronsted-Lourijeva kiselina.
Zatim je 1963. slijedio koncept klasifikacije u jake i slabe baze i kiseline. Jačina interkacija između Luisovih baza i kiselina se mjeri standardnom entalpijom stvaranja adukta i može biti predviđena Drago-Vajlandovom jednačinom sa dva parametra.
Reformulacija Luisove teorije[uredi | uredi kod]
Luis je 1916. godine predložio koncept po kome se hemijska veza stvara tako što dva atoma dijele zajednički elektronski par koji ih drži na okupu. Kada svaki atom doprinese sa pojednim svojim elektronom onda se zove kovalentna veza. Kada oba elektrona dolaze od samo jednog od atoma onda se veza naziva dativna kovalentna ili koordinatna veza. Razlika između ovih veza nije čvrsta. Tako na primjer tokom formiranja amonijum jona između amonijaka i vodonika molekul amonijaka donira elektronski par jonu vodonika, ali identitet elektrona je izgubljen u amonijum jonu koji je formiran. Luis je takođe predložio da donor elektronskog para bude klasifikovan kao baza a akceptor elektronskog para kao kiselina.
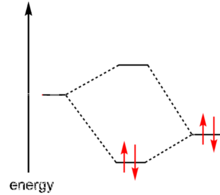
Moderna definicija Luisove kiseline ja da je to atomska ili molekulska vrsta koja ima lokalizovanu praznu atomsku ili molekulsku orbitalu. Molekulska orbitala sa najnižom energijom (LUMO) može primiti elektronski par.
Upoređivanje sa Bronsted-Lourijevom teorijom[uredi | uredi kod]
Luisova baza je često i Bronsted-Lourijeva baza pošto može donirati elektronski par protonu, proton je Luisova kiselina pošto može prihvatiti elektronski par. Konjugovana baza Bronsted-Lourijeve kiseline je takođe Luisova baza pošto nakon gubitka protona iz kiseline na mjestu gdje je bila veza A—H ostaje slobodni elektronski par na konjugovanoj bazi. Luisove baze se mogu teško protonizovati ali reaguju sa Luisovim kiselinama. Na primjer ugljen monoksid je slaba Bronsted-Lourijeva baza ali formira jak adukt sa BF3.
2,6-di-t-butilpiridin reaguje sa HCl pri čemu se formira hidrohloridna so ali ne reaguje sa BF3. Ovaj primjer pokazuje da sterni faktori u kombinaciji sa elektronskim faktorom igra ulogu u određivanju jačine interakcije između glomaznog di-t-butilpiridina i malog protona.
Bronsted-Lourijeva kiselina je donor protona, a ne akceptor elektronskog para.
Luisove kiseline[uredi | uredi kod]

Postoje razne vrste Luisovih kiselina. Najjednostavnije su one koje reaguju direktno sa Luisovom bazom ali češće su one koje prvo stupaju u reakciju prije nego što se formira adukt.
Jednostavne Luisove kiseline[uredi | uredi kod]
Najčešći primjer takvih kiselina su bor-trihalidi i organska jedinjenja bora:
- BF3 + F- → BF4−
U ovom aduktu se sve četiri fluoridine grupe (tj. ligandi) ekvivalentne.
- BF3 + OMe2 → BF3OMe2
I BF4- i BF3OMe2 su adukti Luisove baze od bor-trifluorida. U mnogim slučajevima adukti krše pravilo okteta kao u slučaju trijodidnog anjona:
- I2 + I- → I3−
Različite boje rastvora joda potiču od različitih mogućnosti rastvarača da formira adukt sa Luisovom kiselinom I2.
U nekim slučajevima je Luisova kiselina u mogućnosti da veže dvije Luisove baze, poznati primjer toga je formiranje heksafluorsilikata:
- SiF4 + 2 F− → SiF62−
Kompleksne Luisove kiseline[uredi | uredi kod]
Mnoga jedinjenja koja se svrstavaju u Luisove kiseline zahtijevaju aktivacioni korak prije nego što se formira adukt sa Luisovom bazom. Poznati primjer je aluminijum-trihalidi, koji su Luisove kiseline. Aluminijum-trihalidi za razliku od bor-trihalida ne postoje u obliku AlX3, nego kao agregati i polimeri koji moraju biti razgrađeni od strane Luisove baze. Jednostavniji slučaj je formiranje adukta borana. Ne postoji monomerni BH3 tako da se adukti borana dobijaju razgrađivanjem diborata:
- B2H6 + 2 H− → 2 BH4−
U ovoj reakciji može biti izolovan intermedijer B2H7−.
Mnogi metalni kompleksi se ponašaju kao Luisove kiseline ali obično nakon što se disosuju sa slabo vezanom Luisovom bazom, obično vodom.
[Mg(H2O)6]2+ + 6 NH3 → [Mg(NH3)6]2+ + 6 H2O
Proton kao Luisova kiselina[uredi | uredi kod]
Proton (H+) je jedna od najjačih ali takođe i jedna od najkomplikovanijih Luisovih kiselina. Konvencija je da se ignoriše da je proton teško rastvoren (tj. vezan za rastvarača). Sa ovim pojednostavljenjem reakcija kiseline i baze tj. formiranje adukta se može predstaviti kao:
- H+ + NH3 → NH4+
- H+ + OH- → H2O
Primjena Luisovih kiselina[uredi | uredi kod]
Tipični primjer primjene Luisove kiseline je reakcija Frider-Kraft alkilacije. Glavni korak ja kada AlCl3 prihvati slobodni elektronski par od hloridnog jona Cl-, pri čemu se formira AlCl4- i stvara se jaka kiselina tj. elektrofilni karbonijum katjon R+.
- RCl +AlCl3 → R+ + AlCl4−
Luisove baze[uredi | uredi kod]
Luisova baza je atomska ili molekulska vrsta gdje je HOMO molekulska orbitala visoko lokalizovana tj. popunjena. Tipične Luisove baze su obični amini kao što su amini amonijaka i alkila. Druge česte Luisove baze uključuju piridin i njegove derivate. Neke od glavnih klasa Luisovih baza su:
- Amini formule NH3-xRx gdje je R alkil ili aril grupa. Tu spadaju i piridini i njegovi derivati.
- Fosfini formule PR3-xArx gdje je R alkil grupa a Ar aril grupa.
- Jedinjenja koja sadrže O, S, Se i Te u oksidacionom stanju 2, uključujući vodu, etre i ketone.
Najčešće Luisove baze su anjoni. Jačina Luisove baze se poklapa sa pKa roditeljske kiseline: kiseline sa visokim pKa daju dobre Luisove baze.
Jačina Luisovih baza je određena za različite Luisove kiseline kao što su I2, SbCl5, i BF3.
| toplota vezivanja različitih baza za bor-trifluorid BF3 | ||
|---|---|---|
| Luisova baza | atom donora | Entalpija stvaranja kompleksa (kJ/mol) |
| Et3N | N | 135 |
| kviniciklidin | N | 150 |
| piridin | N | 128 |
| acetonnitril | N | 60 |
| Et2O | O | 78.8 |
| THF | O | 90.4 |
| aceton | O | 76.0 |
| EtOAc | O | 75.5 |
| DMA | O | 112 |
| DMSO | O | 105 |
| tetrahidrotiofen | S | 51.6 |
| PMe3 | P | 97.3 |
Primjena Luisovih baza[uredi | uredi kod]
Skoro sva jedinjenja koja sadrže prelazne metale su Luisove baze tj. ligandi, koje su vezane za metal. Važna primjena Luisovih baza je da modifikuju aktivnost i selektivnost katalizatora. Zbog toga Luisove baze mogu uzrokovati hiralnost na katalizatoru, omogućujući asimetričnu katalizu, što je korisno u proizvodnji farmaceutskih sredstava.
Mnoge Luisove baze mogu formirati višestruke veze sa Luisovom kiselinom. Ovakve Luisove kiseline se zovu agensi za helaciju.
Klasifikacija na jake i slabe kiseline i baze[uredi | uredi kod]
Luisove baze i kiseline se obično klasifikuju na osnovu njihove jačine ili slabosti. U ovom kontekstu jak označava mali i nepolarizabilan a slabe označavaju veće atome koji se lakše polarizuju.
- tipične jake kiseline: H+, katjoni alkalnih metala, borani, Zn2+
- tipične slabe kiseline: Ag+, Mo(0), Ni(0), Pt2+.
- tipične jake baze: amonijak i amini, voda, karboksilati, fluoridi i hloridi.
- tipične slabe baze: organofosfini, tioetri, ugljen-monoksid i jodidi.
Na primjer amin će zamijeniti fosfin iz adukta sa kiselinom BF3. Na isti način se mogu klasifikovati i baze. Na primjer baze koje doniraju slobodni elektronski par sa atoma kiseonika su jače nego baze koje doniraju sa atoma azota. Iako ova klasifikacija nije nikada bila kvantifikovana pokazalo se da je vrlo korisna u predviđanju jačine stvaranja adukta pri čemu se koriste ključni koncepti:
- interakcija jaka kiselina-tvrda baza je jača od interakcije jaka kiselina-slaba baza ili slaba kiselina-jaka baza.
- interakcija slaba kiselina-slaba baza je jača od interakcije slaba kiselina-jaka baza ili jaka kiselina-slaba baza.
Dalja istraživanja termodinamike interakcija je pokazala da su interakcija jako-jako favorizovane entalpijski, a reakcije slabo-slabo su entropijski favorizovane.
Literatura[uredi | uredi kod]
- ^ http://goldbook.iupac.org/L03508.html
- ^ a b Miessler, L. M., Tar, D. A., (1991) p166 - Table of discoveries attributes the date of publication/release for the Lewis theory as 1923.
- ^ Brown HC and Kanner B. "Preparation and Reactions of 2,6-Di-t-butylpyridine and Related hindered Bases. A case of Steric Hindrance toward the Proton." J. Am. Chem. Soc. 88, 986 (1966).