Molekulska orbitala
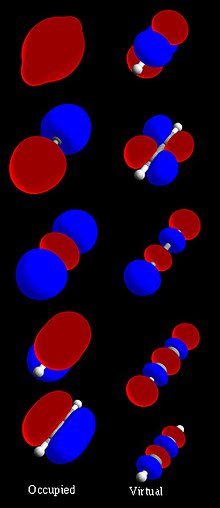
U hemiji, molekulska orbitala (skr. MO) je matematička funkcija koja opisuje ponašanje elektrona kao talasa u molekulu.[1][2][3] Ova funkcija se može koristiti za izračunavanje fizičkih i hemijskih osobina kao što je nalaženje elektrona u određenom dijelu prostora. Molekulske orbitale se najčešće konstruišu kombinacijom atomskih ili hibridnih orbitala svakog od atoma u datom molekulu.[4]
Pregled[uredi | uredi kod]
Molekulska orbitala može da posluži za određivanje elektronske konfiguracije molekula: prostorne distribucije i energije elektrona ili para elektrona. Najčešće se molekulske orbitale prikazuju kao linearna kombinacija atomskih orbitala, naročito pri kvalitativnj ili aproksimativnoj analizi. Ovaj metod je nezamjenljiv za obezbjeđivanje jednostavnog modela veza u molekulu, kao što je slučaj sa teorijom molekulskih orbitala.[5]
Molekulska orbitala opisuje ponašanje jednog elektrona u električnom polju koje stvara jezgro i prosječna raspodjela drugih elektrona. Ako se u orbitali nalaze dva elektrona Paulijev princip isključenja nalaže da moraju imati suprotan spin. Molekulska orbitala predstavlja aproksimaciju i opisi talasne funkcije elektrona u molekulu koji su visoko tačni nemaju orbitale.
Kvalitativni opis[uredi | uredi kod]
Sve talasno mehaničke odnosno talasno mehaničke zakonitosti koje važe za atom, važe i za složeniji sistem — molekul. To znači da su prema ovoj teoriji i metodi elektroni raspoređeni u molekulu kao i u atomu po odgovarajućim orbitalama. Osnovna razlika je što su atomske orbitale monocentrične, a molekulske su policentrične tj. izgrađuju se oko dva ili više atomskih jezgara.
Molekulske orbitale se mogu dobiti metodom linearne kombinacije atomskih orbitala. Kao rezultat kombinacije dvije atomske orbitale, dobijaju se dvije molekulske orbitale predstavljene zbirom odnosno razlikom atomskih orbitala.
Broj molekulskih orbitala je jednak broju atomskih orbitala koje su uključene u linearnu kombinaciju.
Primjeri[uredi | uredi kod]
H2[uredi | uredi kod]


Molekul vodonika se sastoji od dva atoma vodonika koje označavamo sa H' i H". Linearnom kombinacijom 1s' i 1s" atomskih orbitala dobijaju se dvije molekulske orbitale: jedna vezivna i druga antivezivna. Vezivna molekulska orbitala se dobije sabiranjem atomskih orbitala i odgovara stanju sistema u kome se elektron nalazi u vezivnoj oblasti. Antivezivna molekulska orbitala se odnosi na oduzimanje atomskih orbitala i odgovara stanju sistema u kome se elektron nalazi u antivezivnoj oblasti.
Vezivna orbitala je po energiji niža od atomskih orbitala, dok antivezivna orbitala ima veću energiju.
Izgradnju molekula od atoma možemo opisati preraspoređivanjem elektrona iz atomskih u molekulske orbitale.
U molekulu vodonika imaju dva elektrona pri čemu oba elektrona se raspoređuju u vezivnu orbitalu pri čemu sistem postaje niži u energiji. Pri tome je napravljena kovalentna veza.
Red veze se definiše kao broj elektrona u vezivnim orbitalama minus broj elektrona u antivezivnim orbitalama i sve podijeljeno sa dva. U primjeru molekula vodonika imaju dva elektrona u vezivnoj orbitali u nema elektrona u antivezivnim orbitalama, pa je red veze jedan i postoji jedna veza između atoma vodonika.
He2[uredi | uredi kod]
Helijum ima dva elektrona u 1s orbitali u osnovnom stanju. U slučaju hipotetičkog molekula He2, dva elektrona bi popunila vezivnu orbitalu a dva antivezivnu i rezultujuća elektronska gustina ne podržava formiranje veze između atoma i molekul ne postoji. Red veze je nula i veza ne postoji.
Da bi mogla da se uspostavi hemijska veza tj. nagradi molekul jedinjenja potrebno je da broj elektrona u vezivnim orbitalama bude veći nego u antivezivnim.
Molekul HeH bi imao malo manju energiju nego početni atomi, ali veću energetsku prednost tj. manju energiju ima H2 + 2 He, tako da molekul HeH postoji samo kratko.
Energetski dijagrami[uredi | uredi kod]
U slučaju složenijih molekula, talasno mehanički model je pogodan za kvantitivni opis veza, ali ne i za kvalitativni. Zbog toga se uvode energetski dijagrami u kojima se molekulske orbitale predstavljene horizontalnim linijama, pri čemu orbitale koje imaju višu energiju su nacrtane više. Degenerisane orbitale (orbitale sa istom energijom) su predstavljene na istom nivou, ali se između njih nalazi razmak. Elektroni se popunjavaju jedan po jedan pridržavajući se Paulijevog principa isključenja i Hundovog pravila tj. u jednoj orbitali se nalaze maksimalno dva elektrona suprotnog spina, na istom energetskom nivou elektroni se popunjavaju da ima maksimalan broj nesparenih elektrona a zatim se uparuju.

HOMO i LUMO orbitale[uredi | uredi kod]
Najviša popunjena molekulska orbitala se naziva HOMO, a najniža molekulska orbitala koja nije popunjena se naziva LUMO. Razlika između energija HOMO i LUMO molekulskih orbitala se naziva zabranjena zona i može da služi kao mjera za sposobnost pobuđivanja molekula, što je manja energija to je molekul lakše pobuditi.
Reference[uredi | uredi kod]
- ↑ Peter Atkins; Julio De Paula. Atkins’ Physical Chemistry. Oxford University Press, 8th ed., 2006.
- ↑ Yves Jean; Francois Volatron. An Introduction to Molecular Orbitals. Oxford University Press, 1993.
- ↑ Michael Munowitz, Principles of Chemistry, Norton & Company, 2000, pp. 229-233.
- ↑ Gary L. Miessler; Donald A. Tarr. Inorganic Chemistry. Pearson Prentice Hall, 3rd ed., 2004.
- ↑ Catherine E. Housecroft, Alan G, Sharpe, Inorganic Chemistry, Pearson Prentice Hall; 2nd Edition, 2005, pp. 29-33.
Spoljašnje veze[uredi | uredi kod]
- Java molecular orbital viewer shows orbitals of hydrogen molecular ion.
- The orbitron, a visualization of all atomic, and some molecular and hybrid orbitals
- xeo Visualizations of some atomic and molecular atoms
