Enzimska kinetika

Enzimska kinetika je oblast koja izučava brzine hemijskih reakcija katalizovanih enzimima. Proučavanje i poznavanje enzimske kinetike daje uvid u mehanizme po kojima se odvijaju ove reakcije. Između ostalog stiče se uvid i u njihovu ulogu u metabolizmu, u to kako je njihova aktivnost kontrolisana u ćelijama i kako droge i otrovi mogu inhibirati njihovu aktivnost.
Enzimi su molekuli koji upravljaju drugim molekulima-enzimskim supstratima. Supstrati se vezuju za aktivno mesto na enzimu i transformišu se u proizvode kroz niz stupnjeva koji čine mehanizam date enzimske reakcije. Neki enzimi mogu vezivati više supstrata i/ili davati više produkata, a primer za to je proteaza koja delujući na jedan protein daje dva polipeptidna proizvoda. Sa druge strane postoje enzimi kao što je DNK polimeraza, koja vezuje nukleotide u DNK. Iako se ovi mehanizmi uglavnom sastoje od velikog broja stupnjeva, jedan karakterističan stupanj određuje ukupnu kinetiku procesa i zove se odlučujući stupanj. Odlučujući stupanj može biti hemijska reakcija ili strukturna promena enzima ili supstrata, koja prati oslobađanje produkta iz enzima.
Poznavanje strukture enzima ima veliki značaj zato što može nagovestiti kako će se tokom katalize vezivati supstrat i enzim, koje promene će se događati tokom reakcije, pa čak i koja je uloga pojedinačnih aminokiselinskih ostataka u mehanizmu.
Razlikuju se dva tipa enzimskih mehanizama, mehanizme koji uključuju jedan supstrat (monosupstratne mehanizme) i mehanizme koji uključuju veći broj supstrata (polisupstratne). Izučavanja enzimske kinetike sa monosupstratnim mehanizmom kakvu ima enzim triozofosfat izomeraza, imaju za cilj da odrede afinitet vezivanja supstrata od strane enzima. Ukoliko enzim vezuje veći broj supstrata npr. enzim dihidrofolat reduktaza (prikazan na slici), enzimska kinetika nam tada može pružiti informaciju o redosledu vezivanja supstrata i građenja produkata.
Proteinski enzimi nisu jedini biološki katalizatori. U procesima vezanim za RNK kao što su translacija i posttranskripciona modifikacija RNK, učestvuju ribozimi i ribozomi. Glavna razlika između proteinskih enzima i RNK katalizatora je ta što RNK katalizatori učestvuju u dosta manjem broju reakcija, ali se njihovi reakcioni mehanizmi i kinetika, posmatraju na isti način kao kod proteinskih enzima.
Opšti principi[uredi | uredi kod]

U reakcijama katalizovanim enzimima učestvuju isti reaktanti i grade se isti produkti kao u nekatalizovanim reakcijama. Enzimi kao i ostali katalizatori ne menjaju položaj ravnoteže između supstrata i produkata.[1]
Međutim, za razliku od običnih hemijskih reakcija, kod enzimski katalisanih reakcija dolazi do zasićenja enzima i to se naziva saturacione reakcije. Brzina enzimski katalisanih reakcija će rasti sa dodatkom supstrata zato što veći broj aktivnih mesta postaje zauzet. Ovaj rast se nastavlja sve dok enzim u potpunosti ne postane zasićen supstratom, kada brzina dostiže svoj maksimum. Dva najznačajnija kinetička parametra enzimski katalisanih reakcija su brzina kojom enzim postaje zasićen određenim supstratom i maksimalna brzina reakcije koja se može dostići.
Poznavanje ovih parametara je značajno pri sagledavanju ponašanja enzima u ćelijskom okruženju i reagovanja na promene sredine.
Postupci za određivanje brzine enzimski katalisanih reakcija[uredi | uredi kod]

Izučavanje enzima podrazumeva eksperimente kojima se određuju brzine enzimski katalisanih reakcija. Kako se enzim ne troši u reakciji koju katalizuje, da bi se odredila brzina reakcije prate se promene koncentracije kako supstrata tako i produkta. Postoji veći broj metoda za određivanje brzine. Spektrofotometrijske metode prate promenu apsorbancije svetlosti od strane reaktanata odnosno produkata sa vremenom i one su vrlo praktične jer omogućavaju kontinualno merenje brzine. Radiometrijske metode prate ugrađivanje ili oslobađanje radioaktivnosti u cilju merenja količine produkta nagrađene u toku vremena. Radi se o diskontinualnim metodama jer zahtevaju izdvajanje uzorka a obično su vrlo osetljive i omogućavaju merenje veoma niske enzimske aktivnosti.[2] Sličan pristup problemu ima masena spektrometrija pri praćenju ugrađivanja ili oslobađanja stabilnih izotopa u toku prelaska reaktanata u produkte.
Najosetljivije metode koriste mikroskop sa laserom, za posmatranje promena pojedinačnih molekula enzima u toku datih katalitičkih reakcija.
Pri ovim merenjima se koristi i pojava promene u fluorescenciji koenzima ili fluorescentnih boja (dodaju se na određeno mesto na proteinu) kroz mehanizam, što omogućava praćenje pokreta na aktivnom mestu proteina.[3] Na ovaj način stiče se nova predstava o kinetici i dinamici pojedinačnih molekula za razliku od klasične enzimske kinetike, koja posmatra ponašanje velikog broja molekula enzima kao celine.[4][5]
Na grafiku reakcione krive je prikazan uobičajen tok kinetičke krive pri nastajanju produkta, koji se koristi pri izučavanju enzima. Na početku reakcije produkt se formira linernom početnom brzinom, kako reakcija teče brzina se smanjuje zbog utroška supstrata ili nagomilavanja produkta što se na kinetičkoj krivoj vidi kao odstupanje od linearnosti. Dužina linearnog dela zavisi od radnih uslova, a može se kretati od milisekunde do sata. Obično se uslovi podešavaju tako da oblast grafika gde je brzina linearna traje više od minuta čime se olakšava rad.
Većina izučavanja enzimske kinetike koriste ovaj inicijalni, linerni deo enzimske reakcije. Takođe je moguće meriti celokupnu reakcionu krivu, a zatim podatke fitovati pomoću nelinearne jednačine brzine. Ovaj metod merenja naziva se analiza progresivne krive[6] i koristi se kao alternativa pri brzim reakcijama kada je i inicijalni stupanj previše brz da bi se tačno izmerio.
Monosupstratne reakcije[uredi | uredi kod]
Enzimi reaguju sa jednim supstratom kroz mehanizme koji se zovu monosupstratni mehanizmi. Ovom tipu enzima pripadaju izomeraze kao što su triozofosfat izomeraza ili bisfosfoglicerat mutaza, intramolekularne liaze kao što su adenilat ciklaze i RNK liaze.[7] Međutim, neki od enzima koji vezuju samo jedan supstrat ne reaguju po ovom mehanizmu, npr katalaza. Iako u rekciji učestvuje jedna vrsta supstrata, postojanje izmenjenog enzimskog intermedijera znači da je mehanizam katalaze zapravo ping-pong mehanizam koji je karakterističan za reakcije sa više supstrata.
Mihaelis-Mentenina kinetika[uredi | uredi kod]
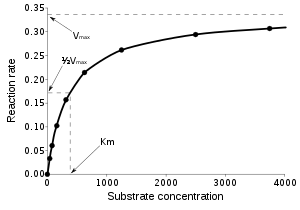
Kako pri enzimski katalisanim reakcijama dolazi do zasićenja enzima, brzina katalitičke reakcije ne pokazuje linearnu zavisnost sa povećanjem koncentracije supstrata. Na krivoj zasićenja vidimo da brzina reakcije (v), raste sa porastom koncentracije supstrata [S] u oblasti niže koncentracije supstrata. Kako [S] raste enzim postaje zasićen supstratom a brzina dostiže svoj maksimum, Vmax.
Mihaelis-Mentenina kinetika za monosupstratnu reakciju je prikazana na slici levo.
Mehanizam počinje bimolekulskom reakcijom između enzima E i supstrata S pri kojoj se gradi kompleks enzim-supstrat, ES. Iako mehanizam monomolekulske reakcije može biti dosta složen, obično postoji jedan odlučujući stupanj za brzinu koji dozvoljava da se mehanizam posmatra kao jedan kinetički stupanj sa konstantom brzine k2.

- (Jednačina 1).
k2 zove se još i kcat ili turnover broj (broj ponavljanja), predstavlja maksimalan broj enzimskih reakcija katalizovanih u sekundi.
Pri nižim koncentracijama supstrata [S] u ravnoteži postoje dva oblika enzima, enzim u slobodnom obliku E i u obliku kompleksa enzim-supstrat, ES. Povećanjem [S] takođe raste i [ES] na račun utroška [E] što ravnotežu pomera na desno. Kako brzina reakcije zavisi od koncentracije ES ona će biti osetljiva na male promene koncentracije supstrata, tako da će pri veoma visokim vrednostima [S] enzim u potpunosti biti zasićen supstratom i postojaće samo u obliku kompleksa ES. Pod ovim uslovima brzina (v≈k2[E]tot=Vmax) je neosetljiva na male promene [S], gde je [E]tot ukupna koncentracija enzima:
što je približno jednako koncentraciji ES pri saturaciji.
Mihaelis-Mentenina jednačina[8] opisuje zavisnost brzine reakcije od položaja ravnoteže pri vezivanju supstrata za enzim i konstante brzine k2. Leonor Mihaelis i Mod Menten su pokazali da se u slučaju da je k2 mnogo manje od k-1 može izvesti sledeća jednačina:
- (Jednačina 2)
Mihaelis-Mentenina jednačina je osnovna kinetička jednačina za monosupstratne enzimske reakcije.
Mihaelisova konstanta, Km je definisana kao koncentracija supstrata pri kojoj je brzina reakcije jednaka polovini Vmax. Ovo možemo proveriti zamenom [S] = Km u Mihaelis-Menteninu jednačinu. Ukoliko je brzina odlučujućeg stupnja mala u poređenju sa disocijacijom supstrata (k2 << k-1), Mihaelisova konstanta je približno jednaka konstanti disocijacije kompleksa ES, mada je ovaj slučaj relativno redak.
Uobičajen slučaj je onaj u kome je k2 > k-1 poznat kao Brigs-Haldanova kinetika.[9] Mihaelis-Mentenina jednačina i dalje važi pod ovim uopštenijim uslovima, kao što se može izvesti iz aproksimacije stacionarnog stanja. U toku inicijalnog perioda možemo smatrati da je brzina reakcije konstantna, a samim tim i da je [ES] skoro konstantno (vidi jednačinu 1.):
gde je Mihaelisova konstanta data kao:
([E] je koncentracija slobodnog enzima). Ako sve ovo uzmemo u obzir, opšta formula za brzinu reakcije v, biće ponovo data Mihaelis-Menteninom jednačinom:
Katalitička efikasnost je mera efikasnosti pri prevođenju supstrata u produkt. Koristeći definiciju Mihaelisove konstante, , Mihaelis-Mentenina jednačina može biti napisana u sledećem obliku:
gde je [E] koncentracija slobodnog enzima. Stoga, specifična konstanta je zapravo konstanta brzine za bimolekularnu reakciju slobodnog enzima i slobodnog supstrata kada nastaje produkt. Specifična konstanta zavisi od učestalosti reakcija enzima i supstrata u rastvoru a vrednosti joj se kreću oko 1010 M−1 s−1 na temperaturi od 25 °C. Značajno je da ovaj maksimum ne zavisi od veličine ni supstrata ni enzima. Odnos specifičnih konstanti dva različita supstrata, odgovara kvantitativnom poređenju efikasnosti kojima enzim transformiše odgovarajuće supstrate. Specifična konstanta se može očitati kao nagib Mihaelis-Mentenine prave pri niskim vrednostima koncentracije supstrata [S] (kada je [S] << Km).
Linearna zavisnost Mihaelis-Menten jednačine[uredi | uredi kod]

Grafik zavisnosti 1/v od 1/[S] je linearan. Iako je na početku, pri niskim koncentracijama supstrata linearan, pri visokim vrednostima [S] kada dolazi do saturacije prava linija postaje kriva. Nelinearnost je predstavljala problem pri određivanju Km i Vmax pre nego što je počela upotreba nelinearnog fitovanja krivih. Zbog toga je nekoliko naučnika razvilo linearizaciju Mihaelis-Mentenine jednačine putem Lajnviver-Burkovog grafika, Edi-Hofsteovog dijagrama i Hanes-Vulfovog grafika.
Lajnviver-Burkov grafik ili dvostruko recipročan grafik je uobičajen način prikazivanja kinetičkih podataka i koristi recipročne vrednosti brzine reakcije i koncentracije supstrata. Kao što se može uočiti, grafik zavisnosti
ima linearan oblik, gde je odsečak na y osi, 1/Vmax, a odsečak na x osi, -1/Km. Kako eksperimentalne vrednosti ne mogu biti negativne, najniža granična vrednost 1/[S] = 0 (presek sa y osom) odgovara beskonačnoj koncentraciji supstrata kada je 1/v=1/Vmax što se vidi na grafiku. Stoga, presek sa x osom je ekstrapolacija eksperimentalnih podataka dobijenih za pozitivne koncentracije. Nedostatak Lajnviver-Burkove metode je u tome što se fokusira na merenja pri niskim koncentracijama supstrata i na taj način unosi grešku pri određivanju Vmax i Km.[10] Tačnija metoda za dobijanje linearnog grafika je Edi-Hofsteova metoda mada su u savremenijem radu pomoću računara sve ove linearizacije zamenjene preciznijim nelinearnim regresionim metodama. Podaci koje daju ove normalizacije omogućavaju smanjenje količine eksperimentalnog rada i povećanje pouzdanosti rezultata a mogu se koristiti i za grafičke i za numeričke metode.[11]
Praktični značaj kinetičkih konstanti[uredi | uredi kod]
Ispitivanje kinetike enzimskih reakcija je važno iz dva razloga. Prvo, omogućava nam da objasnimo na koji način enzimi deluju, i drugo, omogućava nam da predvidimo kako se enzimi ponašaju u živim organizmima. Naime, zajedničko delovanje enzima na metaboličke procese se opisuje kinetičkim konstantama koje su označene kao Km i Vmax.
Ova predviđanja nisu jednostavna, čak i u slučaju prostih sistema. Na primer, oksaloacetat se stvara pomoću malat-dehidrogenaze u mitohondrijama. Oksaloacetat može da izreaguje sa citrat sintazom, fosfoenolpiruvat karboksikinazom ili aspartat aminotransferazom ulazeći u ciklus limunske kiseline, glukoneogenezu ili biosintezu asparaginske kiseline. Da bi se predvideo u koji ciklus oksaloacetat ulazi mora se znati koncetracija oksaloacetata kao i koncentraciju i kinetiku svakog od ovih enzima.[12][13]
Polisupstratne reakcije[uredi | uredi kod]
Polisupstratne reakcije se odvijaju preko više reakcionih stupnjeva koji opisuju kako se supstrati vezuju i kojim redosledom. Analiza ovih reakcija je mnogo jednostavnija ako se koncentracija supstrata A održava konstantnom a supstrata B menja. Pod ovim uslovima, enzim se ponaša kao monosupstratni enzim, a grafik zavisnosti brzine reakcije od koncentracije supstrata daje vrednosti konstanti Km i Vmax za supstrat. Ukoliko se ova merenja vrše pri različitim koncentracijama supstrata A, dobijeni podaci se mogu iskoristiti za utvrđivanje mehanizma reakcije. Za enzime koji reaguju sa dva supstrata A i B i time ih prevode u dva produkta P i Q, postoje dva tipa mehanizma: mehanizam tercijarnog kompleksa i ping-pong mehanizam.
Mehanizam ternarnog kompleksa[uredi | uredi kod]
Kod ovih reakcija, oba supstrata se istovremeno vezuju za enzim stvarajući EAB kompleks. Vezivanje supstrata za enzim može biti nasumično odnosno proizvoljno ili se supstrati mogu vezivati određenim rasporedom. Kada se funkcionalna zavisnost brzine reakcije od koncentracije supstrata (stalna koncentracija A i promenljiva koncentracija B, i obratno) prikaže grafički, preko Lajnviver-Burkovog grafika, dobijene linije će se presecati.
Enzimi koji deluju po ovom mehanizmu su glutation S-transferaze[14], dehidrofolat reduktaze[15] i DNK polimeraze[16].
Ping-pong mehanizam[uredi | uredi kod]

Enzimi sa ping-pong mehanizmom mogu postojati u dva oblika, E i hemijski modifikovan oblik enzima E* (intermedijer). U ovom mehanizmu, supstrat A se vezuje za enzim prevodeći ga u modifikovani oblik E* putem, na primer, prenosa hemijske grupe do aktivnog mesta a zatim biva otpušten. Tek nakon otpuštanja prvog supstrata, može se vezati supstrat B koji tada reaguje sa modifikovanim enzimom, vraćajući ga time u nemodifikovani oblik E. Kada se funkcionalna zavisnost brzine reakcije od koncentracije supstrata (stalna koncentracija A i promenljiva koncentracija B, i obratno) prikaže grafički, preko Lajnviver-Burkovog grafika, dobijene linije biće međusobno paralelne.
U enzime sa ping-pong mehanizmom spadaju neke oksidoreduktaze kao što je tioredoksin peroksidaza[17], transferaze kao što je acilneuraminat citidililtransferaza[18] i serin proteaze kao što je tripsin i hemotripsin.[19]. Serin proteaze su raznovrsna grupa enzima i tu spadaju, na primer, enzimi koji učestvuju u varenju, nekoliko enzima koji učestvuju u zgrušavanju krvi i mnogi drugi. U ovim serin-proteazama energetski aktiviran intermedijer je vrsta acil-enzima, koji je formiran dejstvom aktivnog mesta bočnog niza serina na peptidnu vezu u proteinskom supstratu.
Kinetika koja ne podleže Mihaelis-Menten mehanizmu[uredi | uredi kod]

Kod nekih enzimskih reakcija, grafička zavisnost brzine reakcije od koncentracije supstrata ima sigmoidalan oblik, koji najčešće ukazuje na kooperativno vezivanje supstrata za aktivno mesto. To znači da vezivanje jednog molekula supstrata utiče na vezivanje narednih molekula. Ovakvo ponašanje je karakteristično za enzime koji imaju po nekoliko interagujućih aktivnih mesta.[20] Tipičan primer ovakvih enzima je hemoglobin kod koga vezivanje supstrata za jedno aktivno mesto menja afinitet ostalih aktivnih mesta da vezuju supstrat.
Pozitivna kooperativnost se javlja kada vezivanje prvog molekula supstrata povećava afinitet drugih aktivnih mesta. Negativna kooperativnost se javlja kada vezivanje prvog supstrata smanjuje afinitet enzima ka vezivanju drugih supstratnih molekula. U alosterne enzime koji pokazuju negativnu kooperativnost[21] ulaze tirozil tRNK-sintaze sisara, dok pozitivnu kooperativnost pokazuju bakterijske aspartat transkarbamilaze[22] i fosfofruktokineze[23].
Kooperativnost je uobičajena pojava i pomaže u regulaciji odgovora enzima na promene u koncentraciji njihovih supstrata. Pozitivna kooperativnost čini enzime mnogo više osetljivim na promene koncentracije supstrata i njihove aktivnosti mogu pokazivati velike promene u uskom opsegu koncentracije supstrata. Obrnuto, negativna kooperativnost čini enzime neosetljivim na male promene koncentracije supstrata.
Za kvantitativno određivanje stepena kooperativnosti najčešće se koristi Hilova jednačina.[24] Na osnovu vrednosti Hilovog koeficijenta n možemo zaključiti na koji način vezivanje supstrata za jedno aktivno mesto utiče na vezivanje ostalih supstrata. Naime, ukoliko je n<1 imamo negativnu kooperativnost, dok ukoliko je n>1 imamo pozitivnu kooperativnost.
Predstacionarno kinetičko stanje[uredi | uredi kod]

U prvom trenutku reakcije enzima sa supstratom, nijedan produkt nije stvoren i ne javljaju se intermedijerne vrste. Ovakvo stanje sistema se naziva predstacionarno stanje. Predstacionarno stanje prema tome učestvuje u formiranju i trošenju enzim-supstrat intermedijera (kao što su ES i E*) sve do uspostavljanja njihovih neravnotežnih stacionarnih koncentracija.
Ovakav prilaz je prvo bio primenjen na reakcije hidrolize katalisane hemotripsinom. Veoma često, otkriće neke intermedijerne vrste je presudno u ispitivanju mehanizma enzimske reakcije. Na primer, u slučaju hemotripsina[25], vezivanjem supstrata za nukleofilni serin koji je deo aktivnog mesta stvara se acil-enzim intermedijer.
Sa grafika zavisnosti količine stvorenih produkata od vremena vidimo da se u prvih par sekundi reakcije intermedijer E*[26] stvara veoma brzo, a zatim se brzina smanjuje sve do uspostavljanja stacionarnog stanja sistema. Ova brza kratka faza reakcije meri jedan katalitički ciklus. Prema tome, količina produkata oslobođena u ovoj fazi i na grafiku prikazana kao presek sa y osom takođe daje količinu upotrebljivog enzima.[27]
Hemijski mehanizam[uredi | uredi kod]
Jedan od važnijih ciljeva merenja kinetike enzimskih procesa je određivanje hemijskog mehanizma neke enzimske reakcije tj. redosled hemijskih stupnjeva koji transformisu supstrat u proizvod. Kinetički procesi koji su dati kao primer u daljem tekstu razmatraju još i kojom se brzinom intermedijeri stvaraju ali ne mogu tačno definisati šta su ti intermedijeri.
Merenja kinetike datih reakcija sprovedena pod različitim uslovima ili sa neznatno modifikovanim enzimima ili supstratima mogu često dati uvid u hemijski mehanizam, zato što određuju najsporiji stupanj ili intermedijere u reakciji. Na primer, raskidanje kovalentne veze između vodonikovog atoma i ostatka molekula je često odlučujući stupanj reakcije. Zamenom jednog po jednog vodonikovog atoma deuterijumima i praćenjem brzine reakcije zamene može se odrediti koji tačno vodonikov atom učestvuje u najsporijem stupnju. Brzina će se promeniti kada vodonik koji učestvuje u odlučujućem stupnju bude zamenjen, zbog primarnih kinetičkih izotopskih efekata koji se dešavaju zato što je veze sa deuterijumom mnogo teže raskinuti nego veze sa vodonikom.[28] Takođe je moguće meriti slične efekte kod drugih izotopskih supstitucija, kao što su 13C/12C i 18O/16O, ali ovi efekti su mnogo manje izraženi.[29]
Izotopski efekti još mogu biti iskorišćeni da objasne različite etape prelaza molekula supstrata u finalne proizvode. Na primer, ponekad je veoma teško utvrditi poreklo atoma kiseonika u finalnom proizvodu; budući da mogu poticati iz vode ili iz dela supstrata. To može biti određeno sistematskom zamenom stabilnog izotopa kiseonika 18O nekim od molekula koji učestvuju u reakciji, a zatim se proverava prisutnost izotopa u proizvodu.[30] Hemijski mehanizam takođe može biti razjašnjen ispitivanjem kinetičkih i izotopskih efekata pod različitim pH uslovima[31], zamenom metalnih jona ili drugih vezanih koenzima[32], prostorno određenom mutagenezom očuvanih ostataka aminokiseline ili ispitivanjem ponašanja enzima u prisustvu analoga supstrata.[33]
Inhibicija enzima[uredi | uredi kod]

Inhibitori enzima su molekuli koji smanjuju ili dovode do gubitka aktivnosti enzima. Mogu biti reverzibilni (njihovim uklanjanjem enzimi ponovo stiču prvobitnu aktivnost) ili ireverzibilni (njihovo dejstvo dovodi do trajne neaktivnosti enzima).
Reverzibilni inhibitori[uredi | uredi kod]
Vrste reverzibilnih inhibicija su: kompetitivne, nekompetitivne, bez inhibicije i mešovite, što zavisi od dejstva inhibitora na Km i Vmax. Ovi različiti efekti su posledica vezivanja inhibitora za enzim E, za kompleks enzim-supstrat ES, ili za oba. Ispitivanjem kinetike enzima u funkciji koncentracije inhibitora možemo zaključiti o kom se tipu inhibitora radi. Naime, ukoliko ovu zavisnost prikazemo putem Lajnviver-Burkovog i Edi-Hofsteovog grafika[10], možemo videti da se u slučaju sva četri tipa inhibicije promena kinetike enzima vrši na sebi svojstven način. Jednostavnosti radi, u upotrebi su dva simbola:
- i
gde su Ki i K'i konstante disocijacije procesa vezivanja inhibitora za enzim i za kompleks enzim-supstrat, respektivno. U prisutstvu reverzibilnog inhibitora, prividne konstante Km i Vmax postaju (α/α')Km i (1/α')Vmax, respektivno, kao što je pokazano u tabeli za pojedinačne slučajeve:
| Tip inhibicije | Km prividno | Vmax prividno | ||
| Ki | () | kompetitivna | ||
| Ki' | () | nekompetitivna | ||
| Ki = Ki' | () | bez inhibicije | ||
| Ki ≠ Ki' | () | mešovita |
Nelinearni regresioni fit podataka za enzimsku kinetiku prema jednačini[34] brzine reakcije može voditi tačnoj proceni konstanti disocijacija Ki i K'i.
Ireverzibilni inhibitori[uredi | uredi kod]
Dejstvo inhibitora može biti i ireverzibilno. Naime, oni mogu izazvati trajnu neaktivnost enzima i to obično preko promene kovalentnih veza na aktivnom mestu. Ove reakcije imaju eksponencijalno opadajući tok i obično su saturacione. Pre saturacije, one su reakcije prvog reda u odnosu na inhibitor.
Mehanizmi katalize[uredi | uredi kod]

Najčešće korišćen model za interakciju enzima i supstrata je indukovani fit model.[35] Po ovom modelu početna interakcija između enzima i supstrata je relativno slaba, ali ova slaba interakcija brzo izaziva konformacione promene enzima koje omogućavaju jače vezivanje supstrata. Ove promene takođe dovode katalitičke ostatke na aktivna mesta u blizini hemijske veze u supstratu, koje će biti promenjene u reakciji.[36] Pošto se završi vezivanje, jedan ili više mehanizma katalize snižavaju energiju prelaznog stanja, omogućavajući alternativni put reakcije. Mehanizmi katalize podrazumevaju katalizu putem: deformacije veze, približavanja i orijentacije, putem proton-donora ili proton-akceptora aktivnih mesta, kovalentnom katalizom i kvantnim tunelovanjem.[26][37]
Enzimska kinetika ne može da pokaže koji je mod katalize korišćen od strane enzima. Ipak, neki kinetički podaci mogu da predvide mogućnosti koje mogu biti ispitivane drugim tehnikama. Na primer, ping-pong mehanizam ukazuje da bi kovalentna kataliza mogla biti važna za enzimski mehanizam. Takođe, uočen jak efekat pH na Vmax ali ne na Km može da ukazuje na to da ostatak na aktivnom mestu mora da bude u određenom jonizacionom stanju da bi se katalitički proces odigrao.
Vidi još[uredi | uredi kod]
Reference[uredi | uredi kod]
- ↑ Ebbing, D.D. General chemistry (4th edition) Houghton Mifflin Co. 1993, ISBN 0-395-63696-5
- ↑ (en)Eisenthal R. Danson M.J. (Eds), Enzyme Assays: A Practical Approach. Oxford University Press (2002) ISBN 0-19-963820-9
- ↑ (en)Xie XS, Lu HP. Single-molecule enzymology. Arhivirano 2009-05-31 na Wayback Machine-u J Biol Chem. 1999 Jun 4;274(23):15967-70. PMID 10347141
- ↑ Lu H (2004). „Single-molecule spectroscopy studies of conformational change dynamics in enzymatic reactions”. Current pharmaceutical biotechnology 5 (3): 261-9. PMID 15180547.
- ↑ Schnell J, Dyson H, Wright P (2004). „Structure, dynamics, and catalytic function of dihydrofolate reductase”. Annual review of biophysics and biomolecular structure 33: 119-40. PMID 15139807.
- ↑ (en)Duggleby, R.G. Analysis of enzyme progress curves by non-linear regression. Methods in Enzymology, (1995) 249:61–90.
- ↑ (en)Hammann C, Lilley DM. Folding and activity of the hammerhead ribozyme. Chembiochem. 2002 Aug 2;3(8):690–700. PMID 11779233
- ↑ (en)Michaelis L. and Menten M.L. Kinetik der Invertinwirkung Biochem. Z. 1913; 49:333–369 English translation Accessed 6 April 2007
- ↑ (en)Briggs GE, Haldane JB. A Note on the Kinetics of Enzyme Action. Biochem J. 1925;19(2):338-9. PMID 16743508
- ↑ 10,0 10,1 (en)Tseng SJ, Hsu JP. A comparison of the parameter estimating procedures for the Michaelis–Menten model. J Theor Biol. 1990 Aug 23;145(4):457–64. PMID 2246896
- ↑ (en)Bravo, I.G., Busto, F., De Arriaga, D., Ferrero, M. A., Rodríguez-Aparicio, L. B., Martínez-Blanco H., Reglero, A.
- A normalised plot as a novel and time-saving tool in complex enzyme kinetic analysis Biochem. J. (2001). 358, 573–583. PMID 11577687
- ↑ (en)Almaas E, Kovacs B, Vicsek T, Oltvai ZN, Barabasi AL. Global organization of metabolic fluxes in the bacterium Escherichia coli. Nature. 2004 Feb 26;427(6977):839-43. PMID 14985762
- ↑ (en)Reed JL, Vo TD, Schilling CH, Palsson BO. An expanded genome-scale model of Escherichia coli K-12 (iJR904 GSM/GPR). Arhivirano 2016-01-29 na Wayback Machine-u Genome Biol. 2003;4(9):R54. PMID 12952533
- ↑ (en)Dirr H, Reinemer P, Huber R. X-ray crystal structures of cytosolic glutathione S-transferases. Implications for protein architecture, substrate recognition and catalytic function. Eur J Biochem. 1994 Mar 15;220(3):645-61. PMID 8143720
- ↑ (en)Stone SR, Morrison JF. Dihydrofolate reductase from Escherichia coli: the kinetic mechanism with NADPH and reduced acetylpyridine adenine dinucleotide phosphate as substrates. Biochemistry. 1988 Jul 26;27(15):5493–9. PMID 3052577
- ↑ (en)Fisher PA. Enzymologic mechanism of replicative DNA polymerases in higher eukaryotes. Prog Nucleic Acid Res Mol Biol. 1994;47:371-97. PMID 8016325
- ↑ (en)Akerman SE, Muller S. 2-Cys peroxiredoxin PfTrx-Px1 is involved in the antioxidant defence of Plasmodium falciparum. Mol Biochem Parasitol. 2003 Aug 31;130(2):75-81. PMID 12946843
- ↑ (en)Bravo, I.G., Barrallo, S., Ferrero, M. A., Rodríguez-Aparicio, L. B., Martínez-Blanco H., Reglero, A. “Kinetic properties of the Acylneuraminate Cytidylytransferase from Pasteurella haemolytica A2”. Biochem. J. (2001) 358, 585-598.
- ↑ (en)Kraut J. Serine proteases: structure and mechanism of catalysis. Annu Rev Biochem. 1977;46:331-58. PMID 332063
- ↑ (en)Ricard J, Cornish-Bowden A. Co-operative and allosteric enzymes: 20 years on. Eur J Biochem. 1987 Jul 15;166(2):255-72. PMID 3301336
- ↑ (en)Ward WH, Fersht AR., Tyrosyl-tRNA synthetase acts as an asymmetric dimer in charging tRNA. A rationale for half-of-the-sites activity. Biochemistry. 1988 Jul 26;27(15):5525–30. PMID 3179266
- ↑ (en)Helmstaedt K, Krappmann S, Braus GH., Allosteric regulation of catalytic activity: Escherichia coli aspartate transcarbamoylase versus yeast chorismate mutase. Microbiol. Mol. Biol. Rev. 2001 Sep;65(3):404-21 PMID 11528003
- ↑ (en)Schirmer T, Evans PR., Structural basis of the allosteric behaviour of phosphofructokinase. Nature. 1990 Jan 11;343(6254):140-5. PMID 2136935
- ↑ (en)Hill, A. V. The possible effects of the aggregation of the molecules of haemoglobin on its dissociation curves. J. Physiol. (Lond.), 1910 40, iv-vii.
- ↑ (en)Hartley B.S. and Kilby B.A. The reaction of p-nitrophenyl esters with chymotrypsin and insulin. Biochem J. 1954 Feb;56(2):288-97. PMID 13140189
- ↑ 26,0 26,1 (en)Alan Fersht, Structure and Mechanism in Protein Science : A Guide to Enzyme Catalysis and Protein Folding. W. H. Freeman, 1998. ISBN 0-7167-3268-8
- ↑ (en)Bender ML, Begue-Canton ML, Blakeley RL, Brubacher LJ, Feder J, Gunter CR, Kezdy FJ, Killheffer JV Jr, Marshall TH, Miller CG, Roeske RW, Stoops JK. The Determination of the Concentration of Hydrolytic Enzyme Solutions : a-Chymotrypsin, Trypsin, Papain, Elastase, Subtilisin, and Acetylcholinesterase. J Am Chem Soc. 1966 Dec 20;88(24):5890-913. PMID 5980876
- ↑ (en)Cleland WW. The use of isotope effects to determine enzyme mechanisms. Arch Biochem Biophys. 2005 Jan 1;433(1):2–12. PMID 15581561
- ↑ Northrop D (1981). „The expression of isotope effects on enzyme-catalyzed reactions”. Annu. Rev. Biochem. 50: 103-31. PMID 7023356.
- ↑ Baillie T, Rettenmeier A (1986). „Drug biotransformation: mechanistic studies with stable isotopes”. Journal of clinical pharmacology 26 (6): 448-51. PMID 3734135.
- ↑ (en)Cleland WW. Use of isotope effects to elucidate enzyme mechanisms. CRC Crit Rev Biochem. 1982;13(4):385–428. PMID 6759038
- ↑ (en)Christianson DW, Cox JD. Catalysis by metal-activated hydroxide in zinc and manganese metalloenzymes. Annu Rev Biochem. 1999;68:33–57. PMID 10872443
- ↑ Kraut D, Carroll K, Herschlag D (2003). „Challenges in enzyme mechanism and energetics”. Annu. Rev. Biochem. 72: 517-71. PMID 12704087.
- ↑ (en)Leatherbarrow RJ. Using linear and non-linear regression to fit biochemical data. Trends Biochem Sci. 1990 Dec;15(12):455–8. PMID 2077683
- ↑ (en)Koshland DE, Application of a Theory of Enzyme Specificity to Protein Synthesis. Proc. Natl. Acad. Sci. U.S.A. 1958 Feb;44(2):98–104. PMID 16590179
- ↑ Hammes G (2002). „Multiple conformational changes in enzyme catalysis”. Biochemistry 41 (26): 8221–8. PMID 12081470.
- ↑ Sutcliffe M, Scrutton N (2002). „A new conceptual framework for enzyme catalysis. Hydrogen tunnelling coupled to enzyme dynamics in flavoprotein and quinoprotein enzymes”. Eur. J. Biochem. 269 (13): 3096-102. PMID 12084049. Arhivirano iz originala na datum 2006-11-08. Pristupljeno 2014-03-03.
Literatura[uredi | uredi kod]
- Athel Cornish-Bowden, Fundamentals of Enzyme Kinetics. (3rd edition), Portland Press 2004, ISBN 1-85578-158-1.
- Irwin H. Segel, Enzyme Kinetics : Behavior and Analysis of Rapid Equilibrium and Steady-State Enzyme Systems. Wiley-Interscience; New Ed edition 1993, ISBN 0-471-30309-7.
- Alan Fersht, Structure and Mechanism in Protein Science : A Guide to Enzyme Catalysis and Protein Folding. W. H. Freeman, 1998. ISBN 0-7167-3268-8
- Santiago Schnell, Philip K. Maini, A century of enzyme kinetics: Reliability of the KM and vmax estimates, Comments on Theoretical Biology 8, 169–187, 2004 DOI: 10.1080/08948550390206768 Arhivirano 2006-02-21 na Wayback Machine-u
- Chris Walsh, Enzymatic Reaction Mechanisms. W. H. Freeman and Company. 1979. ISBN 0-7167-0070-0
- Nicholas Price, Lewis Stevens, Fundamentals of Enzymology, Oxford University Press, 1999. ISBN 0-19-850229-X
- Tim Bugg, An Introduction to Enzyme and Coenzyme Chemistry Blackwell Publishing, 2004 ISBN 1-4051-1452-5
Spoljašnje veze[uredi | uredi kod]
- Animation of an enzyme assay Shows effects of manipulating assay conditions.
- MACiE Arhivirano 2009-09-07 na Wayback Machine-u A database of enzyme reaction mechanisms.
- ENZYME Expasy enzyme nomenclature database.
- ExCatDB Arhivirano 2007-10-13 na Wayback Machine-u A database of enzyme catalytic mechanisms.
- BRENDA Arhivirano 2008-12-11 na Wayback Machine-u Comprehensive enzyme database, giving substrates, inhibitors and reaction diagrams.
- SABIO-RK Arhivirano 2006-11-17 na Wayback Machine-u A database of reaction kinetics.
- Joseph Kraut's Research Group, University of California San Diego. Arhivirano 2006-08-20 na Wayback Machine-u Superb animations of several enzyme reaction mechanisms.
- Symbolism and Terminology in Enzyme Kinetics, A comprehensive explanation of concepts and terminology in enzyme kinetics.
- An introduction to enzyme kinetics Arhivirano 2004-06-12 na Wayback Machine-u An accessible set of on-line tutorials on enzyme kinetics.

![{\displaystyle {\begin{matrix}v=k_{2}[{\mbox{ES}}]\end{matrix}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/befe56463761168b47df5be5bfa796c6d3f6a7dd)
![{\displaystyle [{\mbox{E}}]_{tot}\ {\stackrel {\mathrm {def} }{=}}\ [{\mbox{E}}]+[{\mbox{ES}}]}](https://wikimedia.org/api/rest_v1/media/math/render/svg/e723eb321d042825c947f9b8e0f744fda6c74f73)
![{\displaystyle v={\frac {V_{max}[{\mbox{S}}]}{K_{m}+[{\mbox{S}}]}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/5c10f2bf1084df37a7d7da00198c23d8095e9f9a)
![{\displaystyle {\frac {d}{dt}}[{\mbox{ES}}]=k_{1}[{\mbox{E}}][{\mbox{S}}]-k_{2}[{\mbox{ES}}]-k_{-1}[{\mbox{ES}}]\approx 0}](https://wikimedia.org/api/rest_v1/media/math/render/svg/ebef645de7f075d9999fba79d30e40568a63a5c7)
![{\displaystyle [{\mbox{ES}}]\approx {\frac {[{\mbox{E}}]_{tot}[{\mbox{S}}]}{[{\mbox{S}}]+K_{m}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/a9425177562bf79b3e086de1277d92f7491fe0d9)
![{\displaystyle K_{m}\ {\stackrel {\mathrm {def} }{=}}\ {\frac {k_{2}+k_{-1}}{k_{1}}}\approx {\frac {[{\mbox{E}}][{\mbox{S}}]}{[{\mbox{ES}}]}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/428e7c1efa5baf314c725f64da8b0ef44c0034c3)
![{\displaystyle v=k_{2}[\mathrm {ES} ]={\frac {k_{2}[{\mbox{E}}]_{tot}[{\mbox{S}}]}{[{\mbox{S}}]+K_{m}}}={\frac {V_{max}[{\mbox{S}}]}{[{\mbox{S}}]+K_{m}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/a9684acdfe5ef1343e2bf7dea6cbd0a81cf8f774)


![{\displaystyle v=k_{2}[\mathrm {ES} ]={\frac {k_{2}}{K_{m}}}[{\mbox{E}}][{\mbox{S}}]}](https://wikimedia.org/api/rest_v1/media/math/render/svg/ce445b17dc8f27b81e07db99d3532af0be5c53ee)
![{\displaystyle {\frac {1}{v}}={\frac {K_{m}}{V_{max}[{\mbox{S}}]}}+{\frac {1}{V_{max}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/b7271b5f19abb33ea11c518ab87f98a1d3a0ab10)
![{\displaystyle \alpha =1+{\frac {[{\mbox{I}}]}{K_{i}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/7d05bffbc19ef9047581c87887ae0eea5c11e7fe)
![{\displaystyle \alpha ^{\prime }=1+{\frac {[{\mbox{I}}]}{K_{i}^{\prime }}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/e8b2033b5725a8b85d7425d409192cf11885c199)










