Transesterifikacija
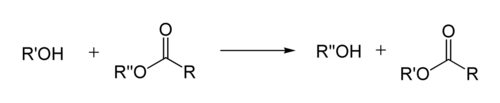
U organskoj hemiji, transesterifikacija je proces zamene organske grupe estra R sa organskom grupom alkohola R′. Ove reakcije su često katalizovane dodavanjem kiseline ili baznog katalizatora. Reakcija se takođe može postići uz pomoć enzima (biokatalizatori), posebno lipaze.
Mehanizam[uredi | uredi kod]
Mehanizam transesterifikacije počinje time što kiseonik iz alkil grupe, napadne vodonik iz druge supstance složene strukture. Reakcija je povratna, pa se može desiti da će se supstanca vratiti na prethodni korak ili nastati supstanca koja sadrži parcijalno pozitivan ugljenik i pozitivno naelektrisan OH+ jon. To je vrlo nepovoljno i nestabilno stanje, pa se alkohol, dodaje kako bi kiseonik iz alkohola napao ugljenik. Ovo je takođe povratna reakcija i kako bi se povećala verovatnoća sudara ugljenika sa kiseonikom, potrebno je staviti razmeru sa većim udelom kiseonika, odnosno alkohola i upravo zato se alkohol tada stavlja u višku. Nakon toga nastaje struktura sa jednom OH grupom, dve alkil grupe, i jednim pozitivno naelektrisanim alkoholom, sa naelektrisanjem na kiseoniku. Kako bi postigao stabilnost, oduzima se H+ jon i nastaje nova relativno nestabilna struktura. Postigla se stabilnost OH jona, pored toga je stabilna i jedna alkil grupa, dok su nestabilni alkoksi i metoksi grupe nestabilne.

S obzirom da se ceo proces transesterifikacije odigrava u kiseloj sredini, jedan vodonik se veže za alkoksi grupu, koja se homolitičko formira u alkohol. S druge strane, ugljenik koji je bio parcijalno naelektrisan, postaje potpuno naelektrisan sa tri veze, što je za njega vrlo nepovoljno, pa se naelektrisanje prebacuje na OH jon koji tada postaje pozitino naelektrisan. Kako bi on postigao stabilnost, kiseonik otpušta vodonik i nastaje dvostruka veza. Konačan proizvod transesterifikacije je estar.