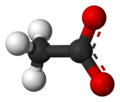
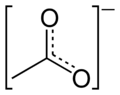
Acetat
Acetat je so sirćetne kiseline.[1] Sirćetna kiselina (CH3COOH) je supstanca rastvorna u vodi, koja stupa u reakcije sa mnogim jedinjenjim.
Acetati se u rastvoru drugačije ponašaju u odnosu na kiselinu od koje potiču. Oni u velikom broju slučajeva posredstvom hidrolize, a uticajem jačeg metalnog jona, poprimaju bazne osobine. Jedinjenja su nestabilna i dešava se da, tokom vremena, određena količina acetata pređe u drugi oblik, a to prati oslobađanje kiseline, čiji se miris oseća pri otvaranju posude u kojoj se ta supstanca nalazi. U strukturnom pogledu, kiselina spada u monokarboksilne kiseline i na karboksilnu grupu je vezana samo jedna metil grupa, koja ima značajan uticaj na reaktivnost čitavog molekula. Elektronegativniji kiseonik ima induktivni efekatprivlačenja elektrona sa susednog ugljenika karboksilne grupe. Samim tim, bogati se elektronima kiseonik, a osiromašuje ugljenik, koji ipak mora to da nadoknadi privlačenjem elektrona, ali znatno slabijim, sa susedne metil grupe. Struktura acetatnog jona je takođe značajna za reaktivnost molekula koji ga sadrži. Kombinacija različitih tipova hibridizacije odigrava značajnu ulogu. Metil grupa je sp3 hibridizovana, a hibridizacija karboksilne grupe je sp2. Ovakva kombinacija omogućava katakterističnu prostornu orijentaciju i različitost u uglovima veza, što pojedine atome jona štiti, a druge navodi na reakciju.
Sama sirćetna kiselina spada u slabe kiseline, pa najlakše reaguje sa jakim bazama kao što su NaOH (natrijum hidroksid, živa soda) i KOH (kalijum hidroksid), gradeći odgovarajuću so (natrijum ili kalijum acetat), pri čemu se izdvaja voda.[1] Pri ovoj reakciji nisu potrebni katalizatori jer se reakcija lako odvija.[2]
- CH3–CH2COOH + NaOH → CH3-CH2COONa + H2O
Voda nastaje reakcijom H+ jona iz COOH grupe i ON- grupe iz natrijum hidroksida. Natrijum acetat se izdvaja pri ovoj reakciji kao beo talog na dnu epruvete. Sirćetna kiselina sa nekom od svojih soli sa alkalnim metalima gradi vrlo stabilne pufere koji se koriste radi postizanja odrečene pH vrednosti. Acetati kao soli jakih baza i sirćetne kiseline reaguju bazno u procesu hidrolize.[1] Postoje slučajevi kada acetati ne reaguju bazno, već neutralno i to približno kod SN3COONH4, gde su oba jona slaba i imaju slične proizvode rastvorljivosti u vodi. Acetati nisu soli sirćetne kiseline samo sa neorganskim bazama. Postoje i organska jedinjenja koja su samo zbog svoje organske prirode nazvana estri, a koja nastaju reakcijom esterifikacije u kojoj učestvuje kiselina i alkohol, u prisustvu najčešće koncentrovane sumporne kiseline. Dolazi do stvaranja estara karakterističnih osobina. Postoji nekliko ogleda koji pokazuju prirodu acetata.[1] Odmeri se približno ista količina natrijum-acetata i vode i to se pomeša, zagreva do ključanja, a potom hladi naglo pod mlazom hladne vode. U tako ohlađenom rastvoru pri dodavanju nekoliko kristala iste soli, dolazi do burne i jasno vidljive kristalizacije.[3][4] Gradi i toksična jedinjenja, a poznat je olovni šećer.
Strukture[uredi | uredi kod]
-
prostor-popunjavajući model acetatnog anjona -
kugla-i-štap model acetatnog anjona -
rezonantni hibrid acetatnog anjona -
kanonički oblici acetatnog anjona
Reflist[uredi | uredi kod]
- ↑ 1,0 1,1 1,2 1,3 McMurry John E. (1992). Fundamentals of Organic Chemistry (3rd izd.). Belmont: Wadsworth. ISBN 0-534-16218-5.
- ↑ Zumdahl, Steven S. (1986). Chemistry. Lexington, Mass: D.C. Heath. ISBN 978-0-669-04529-1.
- ↑ Lide David R., ur. (2006). CRC Handbook of Chemistry and Physics (87th izd.). Boca Raton, FL: CRC Press. 0-8493-0487-3.
- ↑ Susan Budavari, ur. (2001). The Merck Index: An Encyclopedia of Chemicals, Drugs, and Biologicals (13th izd.). Merck Publishing. ISBN 0-911910-13-1.
Literatura[uredi | uredi kod]
- Zumdahl, Steven S. (1986). Chemistry. Lexington, Mass: D.C. Heath. ISBN 978-0-669-04529-1.