Aluminijum hidrid
| Aluminijum hidrid | |||
|---|---|---|---|

| |||
Aluminijum hidrid | |||
| Naziv po klasifikaciji | Aluman | ||
| Drugi nazivi | Alan Aluminijum(III) hidrid | ||
| Identifikacija | |||
| CAS registarski broj | 7784-21-6 | ||
| PubChem[1][2] | 14488 14399066 (2H3) 16721258 (3H3) | ||
| ChemSpider[3] | 13833 | ||
| ChEBI | 30136 | ||
| Gmelin Referenca | 245 | ||
| Jmol-3D slike | Slika 1 | ||
| |||
| |||
| Svojstva | |||
| Molekulska formula | AlH3 | ||
| Molarna masa | 29.99 g/mol | ||
| Agregatno stanje | bela kristalina supstanca, neisparljiva, visoko polimerizovana, iglasti kristali | ||
| Gustina | 1.486 g/cm3, (čvrsto stanje) | ||
| Tačka topljenja |
150 °C | ||
| Tačka ključanja |
razlaže se | ||
| Rastvorljivost u vodi | reaktivan | ||
| Srodna jedinjenja | |||
| Srodna jedinjenja | Litijum aluminijum hidrid | ||
|
Ukoliko nije drugačije napomenuto, podaci se odnose na standardno stanje (25 °C, 100 kPa) materijala | |||
| Infobox references | |||
Aluminijum hidrid je neorgansko jedinjenje sa formulom AlH3. On je bezbojni čvrsti materijal koji je piroforan. Mada se retko sreće van laboratorije, alan i njegovi derivati su korisni kao redukujući agensi u organskoj sintezi.[4]
Struktura[uredi | uredi kod]
Alan je polimer. Njegova formula je nekad prikazuje kao (AlH3)n. Aluminijum hidrid formira brojne polimorfe, koji se nazivaju α-alan, α’-alan, β-alan, δ-alan, ε-alan, θ-alan, i γ-alan. α-Alan ima kubnu ili romboedrsku morfologiju, dok α’-alan formira iglama slične kristale i γ-alan formira snopove spojenih igli. Alan je rastvoran u THF-u i etru, i njegova brzina precipitacije iz etra zavisi od metoda pripreme.[5]
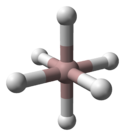
Struktura α-alana je određena. Ona se sastoji od atoma aluminijuma okruženih sa 6 atoma vodonika koji su mostovi sa 6 drugih atoma aluminijuma. Al-H rastojanja su međusobno ekvivalentna (172 pm) i Al-H-Al ugao je 141°.[6]
 |
 |
 |
α-Alan je termički najstabilniji polimorf. β-alan i γ-alan se formiraju zajedno, i konvertuju do α-alana nakon zagrevanja. δ, ε, i θ-alan se formiraju u različitim kristalizacionim uslovima. Mada su oni manje termički stabilni, oni se ne konvertuju u α-alan nakon zagrevanja.[5]
Literatura[uredi | uredi kod]
- ↑ Li Q, Cheng T, Wang Y, Bryant SH (2010). „PubChem as a public resource for drug discovery.”. Drug Discov Today 15 (23-24): 1052-7. DOI:10.1016/j.drudis.2010.10.003. PMID 20970519.
- ↑ Evan E. Bolton, Yanli Wang, Paul A. Thiessen, Stephen H. Bryant (2008). „Chapter 12 PubChem: Integrated Platform of Small Molecules and Biological Activities”. Annual Reports in Computational Chemistry 4: 217-241. DOI:10.1016/S1574-1400(08)00012-1.
- ↑ Hettne KM, Williams AJ, van Mulligen EM, Kleinjans J, Tkachenko V, Kors JA. (2010). „Automatic vs. manual curation of a multi-source chemical dictionary: the impact on text mining”. J Cheminform 2 (1): 3. DOI:10.1186/1758-2946-2-3. PMID 20331846.
- ↑ Brown, H. C.; Krishnamurthy, S. Tetrahedron 1979, 35, 567.
- ↑ 5,0 5,1 Lund, Gary K., Hanks, Jami M., Johnston, Harold E., US Patent and Trade Office, 2007, Pat. Application # 20070066839
- ↑ Turley J W,. Rinn H W (1969). „The crystal structure of aluminum hydride”. Inorganic Chemistry 8 (1): 18–22. DOI:10.1021/ic50071a005.