Elektroliza
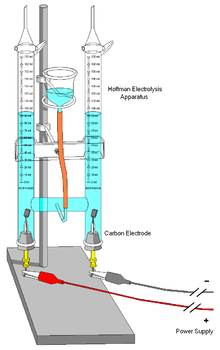
Elektroliza je oblik analize koji se vrši pomoću električne struje.
Opis i princip rada[uredi | uredi kod]
Možemo raščlanjivati samo tvari čije vodene otopine ili taline provode električnu struju. Takve se tvari nazivaju elektrolitima, a dijele se na jake i slabe. Elektrolit se ulije u elektrolizer (posudu u kojoj se vrši elektroliza) i u njega se urone elektrode spojene na izvor istosmjerne električne struje. Zbog prolaska struje kroz elektrolit, ioni otopine ili taline kreću se prema elektrodama. Katione (pozitivne čestice) privlači katoda (negativna elektroda), a anione (negativne čestice) anoda (pozitivna elektroda). Na elektrodama se počinju vršiti elektrodne reakcije – redukcija na katodi i oksidacija na anodi. Ako je moguće više istovremenih različitih elektrodnih reakcija, odvijat će se ona za koju treba najmanje energije. Kod svih metala čiji je standardni redukcijski elektrodni potencijal veći od -1.5V, elektrolizom vodenih otopina njihovih soli na katodi se vrši redukcija iona tih metala. Ako je standardni redukcijski elektrodni potencijal manji od -1.5V, na katodi se vrši redukcija vode. Na anodi se tijekom elektrolize vodenih otopina soli koje sadrže jednostavne anione uvijek vrši oksidacija tih aniona. Ako soli sadrže složene ione, na anodi se uvijek vrši oksidacija vode.[1]
Elektroliza vode[uredi | uredi kod]
Elektroliza vode se koristi pretežno za dobivanje vodika. Voda koja se koristi ne smije biti destilirana (jer takva voda ne provodi električnu struju), pa se u nju često dodaje malo kuhinjske soli. Elektrode moraju biti napravljene od platine jer bi nastali kisik reagirao s većinom ostalih metala. Na katodi se vrši redukcija i nastaje vodik (u plinovitom stanju): "H2O + 2e- → H2 + 2OH-, a na anodi oksidacija pri kojoj nastaje kisik (također kao plin): 2H2O → O2 + 4e- + 4H+. Konačna formula te reakcije glasi 2H2O → 2H2 + O2.
Primjeri[uredi | uredi kod]
Elektroliza vodene otopine bakrovog(II) klorida (CuCl2)[uredi | uredi kod]
U laboratorijsku čašu ulijemo otopinu CuCl2, u kojoj je bakrov(II) klorid disocirao na Cu2+ i Cl- ione. U otopinu uronimo elektrode i spojimo ih na Leclancheov članak (ili koji drugi izvor istosmjerne električne struje). Cu2+ ioni su privučeni prema katodi, gdje dobiju po dva elektrona te nastaje elementarni bakar: Cu2+ + 2e- → Cu. Istodobno su Cl- ioni privučeni prema anodi, gdje otpuštaju po elektron te nastaje je elementarni klor: 2Cl- → Cl2 + 2e-. Nakon nekog vremena, na anodi se počinju pojavljati mjehurići plina karakterističnog mirisa – klora, a katoda poprimi bakreno-crvenu boju – nakupljeni bakar iz otopine. Taj bakar operemo u dušičnoj kiselini.
Cijela jednadžba reakcije izgleda ovako:
Cu2+ + 2e- → Cu
2Cl- → Cl2 + 2e-
Cu2+ + 2Cl- → Cu + Cl2
Elektroliza vodene otopine modre galice (CuSO4)[uredi | uredi kod]
U laboratorijsku čašu ulijemo otopinu CuSO4, u kojoj je modra galica disocirala na Cu2+ i SO42- ione. U otopinu uronimo elektrode i spojimo ih na Leclancheov članak (ili koji drugi izvor istosmjerne električne struje). Cu2+ ioni su privučeni prema katodi, gdje dobiju po dva elektrona, pri čemu nastaje elementarni bakar: Cu2+ + 2e- → Cu. Istodobno se SO42- ioni nakupljaju u anodnom prostoru i ne oksidiraju, nego se, zbog manje uložene energije, oksidira voda: 2H2O → O2 + 4e- + 4H+. Nakon nekog vremena, na katodi se počinju pojavljati mjehurići plina – kisika, a katoda poprimi bakreno-crvenu boju – nakupljeni bakar iz otopine. Taj bakar operemo u dušičnoj kiselini.
Cijela jednadžba reakcije izgleda ovako:
Cu2+ + 2e- → Cu
2H2O → O2 + 4e- + 4H+
2Cu2+ + 2H2O → 2Cu + O2 + 4H+
Elektroliza vodene otopine kuhinjske soli (NaCl)[uredi | uredi kod]
Na metalni stalak pričvrstimo U-cijev i u nju staklenim lijevkom ulijemo otopinu, u kojoj je sol disocirala na Na+ i Cl- ione. U oba kraja U-cijevi kapaljkom stavimo nekoliko kapi fenolftaleina. Svaku elektrodu uronimo u jedan kraj U-cijevi i spojimo s Leclancheovim člankom (ili kojim drugim izvorom istosmjerne električne struje). Na katodi se reducira voda, a ne Na+ ioni (koji se nakupljaju u katodnom prostoru) jer je za to potrebno manje energije: 2H2O + 2e- → H2 + 2OH-. OH- ioni se također nakupljaju u katodnom prostoru te reagiraju s kationima natrija čineći natrijevu lužinu (Na+OH-). Zbog toga smjesa oko anode postaje ljubičasta - fenolftalein dokazuje prisustvo baze. Na anodi oksidiraju ioni klora: 2Cl- → Cl2 + 2e-, koji se vidi u obliku mjehurića i osjeti se njegov karakterističan miris.
Cijela jednadžba reakcije izgleda ovako:
2H2O + 2e- → H2 + 2OH-
2Cl- → Cl2 + 2e-
2H2O + 2Cl- → H2 + 2OH- + Cl2
+Na+ → +Na+
__________________________
2H2O+2NaCl→ 2NaOH + Cl2 + H2
Reference[uredi | uredi kod]
- ↑ R. J. D. Tilley (2004). Understanding solids: the science of materials. John Wiley and Sons. str. 281–. ISBN 978-0-470-85276-7. Pristupljeno 22 October 2011.
