Faza (termodinamika)
U fizičkim naukama, faza je skup stanja makroskopskih fizikalnih sistema koji imaju relativno unifoman hemijski sastav i fizičke osobine (npr. gustoću, kristalnu strukturu, indeks prelamanja, itd.).[1][2]:86[3] U sistemu koji se sastoji od leda i vode u staklenoj tegli, kocke leda su jedna faza, voda je druga, a vlažni vazduh iznad vode je treća faza. Staklo tegle je još jedna zasebna faza.
Termin faza se ponekad koristi kao sinonim za agregatno stanje materije, mada može da postoji nekoliko faza koje se ne mešaju, iako su u istom agregatnom stanju. Isto tako, termin faza se ponekad koristi za označavanje skupa ravnotežnih stanja razdvojenih faznim granicama na faznom dijagramu izraženih u vidu promenljivih stanja, kao što su pritisak i temperatura. Pošto se fazne granice odnose na promene u organizaciji materije, kao što su promene od tečnog do čvrstog stanja, ili na suptilnije promene jedne kristalne strukture u drugu, ovaj drugi vid primene je sličan primeni "faze" kao sinonima za stanje materije.
Tipovi faza[uredi | uredi kod]
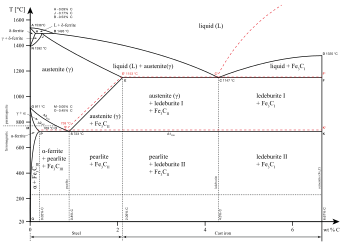
Različite faze sistema mogu se predstaviti korištenjem faznih dijagrama. Ose dijagrama su relevantne termodinamičke promenljive. Za jednostavne mehaničke sisteme, obično se koriste pritisak i temperatura.
Distinktne faze mogu da postoje unutar datog agregatnog stanja materije. Kao što je prikazano na dijagramu leguraa gvožđa, postoji nekoliko faza u čvrstom i tečnom stanju. Faze se isto tako mogu diferencirati po osnovi rastvorljivosti, ne polarne (hidrofilne) i nepolane (hidrofobne). Smeša vode (polarne tečnosti) i ulja (nepolarne tečnosti) se spontano razdvaja u dve faze. Voda ima veoma nisku rastvorljivost (nerastvorna je) u ulju, a ulje ima veoma nisku rastvorljivost u vodi. Rastvorljivost je maksimalna količina rastvorka koji se može rastvoriti u rastvaraču pre nego što rastvora prestane da se rastvara i ostaje u zasebnoj fazi. Smeša se može razdvojiti u više od dve faze. Koncept separacije faza je primenljiv na čvrste materije, i.e., čvrste materije mogu da formiraju čvrste rastvore ili da kristalizuju u distinktne kristalne faze. Metalni parovi koji su uzajamno rastvorni mogu da formiraju legure, dok metalni parivi koji su uzajamno nerastvorni ne mogu.
Postoje sistemi koji sadrže i do osam nemešljivih tečnih faza[4] Uzajamno nemešljive tečne faze se formiraju od vode (vodene faze), hidrofobnih organskih rastvarača, perfluorougljenika (fluorne faze), silikona, nekoliko različitih metala, kao i rastopljenog fosfora. Svi organski rastvarači se ne mešaju, e.g. smeša etilen glikola i toluena se može razdvojiti u dve zasebne organske faze.[5]
Faze ne moraju da se spontano makroskopski razdvajaju. Emulzije i koloidi su primeri nemešljivih faza parova kombinacija koji se fizički ne razdvajaju.
Fazna ravnoteža[uredi | uredi kod]
Kad su prepuštene uravnoteženju, mnoge kompozicije formiraju jednu uniformnu fazu. S druge strane u zavisnosti od temperature i pritiska čak i pojedinačne supstance se mogu razdvojiti u dve ili više zasebnih faza. Svaka faza ima uniformna svojstva, dok su svojstva različitih faza različita.
Voda u zatvorenoj posudi sa vazdušnim prostorom iznad nje formira dvofazni sistem. Najveći deo vode je u tečnoj fazi, gde se održava putem uzajamnog privlačenja molekula vode. Molekuli vode koji su u ravnoteži se konstantno kreću, i povremeno molekul tečne faze stekne dovoljnu kinetičku energiju da se odvoji od tečne faze i uđe u gasnu fazu. Slično tome, s vremena na vreme molekul pare se sudari sa površinom tečnosti i kondenzuje se u tečnost. U ravnoteži, procesi evaporacije i kondenzacije se međusobno balansiraju i nema neto promene zapremine bilo koje faze.
Na sobnoj temperaturi i pritisku, sud sa vodom dostiže ravnotežu kad vazduh nad vodom ima vlažnost od oko 3%. Taj procenat se povećava sa povećanjem temperature. Na 100 °C i atmosferskom pritisku, ravnoteža se ne dostiže dok vazduh ne sadži 100% vode. Ako se tečnost zagreje malo preko 100 °C, prelaz iz tečnosti u gas se javlja ne samo na površini, nego u celoj zapremini tečnosti: voda ključa.
Broj faza[uredi | uredi kod]
- Vidi takođe: Multifazna tečnost
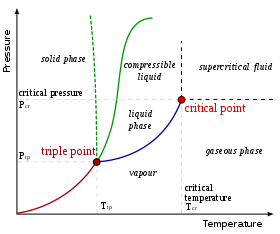
Za datu kompoziciju, samo pojedine faze su moguće na datoj temperaturi i pritisku. Broj i tip faza koji će se formirati je teško predvideti i obično se eksperimentalno određuje. Rezultati takvih eksperimenata se mogu prikazati u obliku faznih dijagrama.
Fazni dijagram koji je ovde prikazan je za jednokomponentni sistem. U tom jednostavnom sistemu, moguće faze zavise samo od pritiska i temperature. Oznake prikazuju tačke gde dve ili više faza mogu da istovremeno postoje u ravnoteži. Na temperaturama i pritiscima koje su udaljene od oznaka, postoji samo jedna faza u ravnoteži.
U dijagramu, plava linija koja označava granicu između tečnosti i gasa se ne produžava neograničeno, nego se završava u tačci koja se naziva kritična tačka. Kad temperatura i pritisak pristupaju kritičnoj tački, svojstva tečnosti i gasa postaju progresivno sve sličnija. U kritičnoj tački, tečnost i gas se ne razlikuju. Iznad kritične tačke, ne postoji više razlika imeđu tečne i gasovite faze: postoji samo generična tečna faza koja se naziva superkritični fluid. U vodi, kritična tačka se javlja oko 647 K (374 °C ili 705 °F) i 22.064 MPa.
Neobično svojstvo vodeneg faznog dijagrama je da linija između čvrste i tečne faze (ilustrovano tačkastom zelenom linijom) ima negativni nagib. Kod većine supstanci, nagib je pozitivan kao što je ilustrovano tamno zelenom linijom. Ovo neobično svojstvo vode je povezano sa manjom gustinom leda od tečne vode. Povećanje pritiska dovodi vodu u fazu veće gustine, što uzrokuje topljenje.
Još jedno interesantno, mada ne i neobično, svojstvo faznog dijagrama je tačka gde se linija čvrste i tečne faze sastaje sa linijom tečne i gasne faze. Presek se naziva trojnom tačkom. U njoj, sve tri faze koegzistiraju.
Eksperimentalno, fazne linije se relativno lako mapiraju usled nezavisnosti temperature i pritiska koji se razvija kad se formiraju višestruke faze. Pogledajte Gibsovo fazno pravilo. Razmotrimo test aparat koji se sastoji od zatvorenog i dobro izolovanog cilindra, na kome je prisutan piston. Menjajući količinu vode i zagrevanja, sistem se može dovesti u bilo koju tačku u gasnom regionu faznog dijagrama. Ako se piston polako snižava, sistem će pratiti krivu povećane temperature i pritiska unutar gasnog regiona faznog dijagrama. U tački gde se gas počne kondenzovati u tečnost, smer krive temperature i pritiska se naglo menja da bi išao duž fazne linije dok se sva voda ne kondenzuje.
Vidite još[uredi | uredi kod]
Reference[uredi | uredi kod]
- ↑ Modell, Michael; Robert C. Reid (1974). Thermodynamics and Its Applications. Englewood Cliffs, NJ: Prentice-Hall. ISBN 0-13-914861-2.
- ↑ Enrico Fermi (25 April 2012). Thermodynamics. Courier Corporation. ISBN 978-0-486-13485-7.
- ↑ Clement John Adkins (14 July 1983). Equilibrium Thermodynamics. Cambridge University Press. ISBN 978-0-521-27456-2.
- ↑ One such system is, from the top: mineral oil, silicone oil, water, aniline, perfluoro(dimethylcyclohexane), white phosphorus, gallium, and mercury. The system remains indefinitely separated at 45 °C, where gallium and phosphorus are in the molten state. From Reichardt, C. (2006). Solvents and Solvent Effects in Organic Chemistry. Wiley-VCH. str. 9–10. ISBN 3-527-60567-3.
- ↑ This phenomenon can be used to help with catalyst recycling in Heck vinylation. See Bhanage, B.M. (1998). „Comparison of activity and selectivity of various metal-TPPTS complex catalysts in ethylene glycol — toluene biphasic Heck vinylation reactions of iodobenzene”. Tetrahedron Letters 39 (51): 9509–9512. DOI:10.1016/S0040-4039(98)02225-4.
Literatura[uredi | uredi kod]
- Сивухин Д. В. Общий курс физики. — Т. II. Термодинамика и молекулярная физика. — 5 изд., испр.. — М.: ФИЗМАТЛИТ, 2005. — 544 с. — ISBN 5-9221-0601-5.
Vanjske veze[uredi | uredi kod]
- French physicists find a solution that reversibly solidifies with a rise in temperature – α-cyclodextrin, water, and 4-methylpyridine
