Horoidalna neovaskularizacija
| Horoidalna neovaskularizacija | |
|---|---|
 | |
| Horoidalna neovaskularizacija u makularnoj degeneraciji oka | |
| Specijalnost | oftalmologija |
| Lečenje | aplikacije anti-VEGF faktora |
| Klasifikacija i eksterni resursi | |
Horoidalna neovaskularizacija (skraćeno CNV) je formiranje novostvorene mikrovaskulaturne mreže, kao reakcija u pokušaju sanacije bolešću izazvane ishemije u unutrašnjem sloju horoideje ili sudovnjače, anatomskog sloja oka bogatog mikrovaskularnom mrežom krvnih sudova. Uobičajenih uzroci neovaskularizacije na mrežnjači (retini) ili u blizini optičkog diska oka su, šećerna bolest, okluzija retinalne vene, i zračenje.[1] Ona je uobičajeni uzrok neovaskularne degenerativne makulopatije (vlažnog oblika makularne degeneracije) [1] ekstremnog oblika kratkovidosti, malignog (teškog) oblika miopije uzrokovane starenjem.[2]
Polazeći od činjenice da je u ovoj bolesti osnovi patogenetskog procesa vaskularna komponenta, zlatni standard u postavljanju dijagnoze je floresceinska angiografija (FA). Ishodh oroidalne neovaskularizacije i izbor terapije direktno zavise od toga da li je membrana ekstrafovealne ili subfovealne lokalizacije. Za ekstrafovealne lezije se koristilaser fotokoagulacija (LPC) i verteporfirinska fotodinamskaterapija (PDT-V). Obe metode su usmerene ka destrukciji CNV, a ne na sprečavanje neoangiogeneze. Membrane subfovealne lokalizacije se dele na tripod tipa: minimalno klasična, predominantno klasična i okultna.[3]
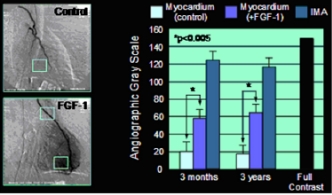
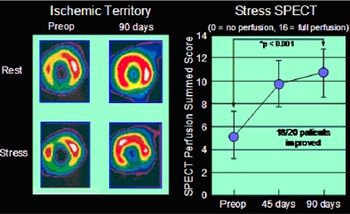
Istovremena pojava angiogeneze i arteriogeneze nedvosmisleno je dokazana na različitim životinjskim modelima,[4][5] kao i kod pacijenata sa koronarnom bolešću.[6] [7]
|
| |
Pojava vaskulogeneze u zrelim organizmima ostaje nerešeno pitanje. Prema dosadašnjim istraživanjima smatra se da je malo verovatno da ovaj proces značajnije doprinosi da se novi krvni sudovi razvijaju ako se taj proces javlja spontano, kao odgovor na ishemiju ili zapaljenja[8] ili kao odgovor na stimulišuće faktore. Tkiva ishemije po sebi ne može biti ključni podsticaj pokretanja angiogenetskog odgovor. Nekoliko pacijenata pokazalo je tu mogućnost u toku hronične ishemije miokarda, ali ne i većina pacijenata sa difuznim mnogostrukim bolestima krvnih sudova kod kojih se ne razvija ishemija na nivou tkiva u odsustvu provokacije. Upala i stres može biti mnogo izraženiji nadražaj,[9][10] i zato se jako mali broj angiogeneze odvija u odsustvo upale.[8] Suzbijanje inflamatornih odgovora, zbog genetskih abnormalnosti, patofiziološkim procesima, ili lekova, može negativno uticati na sposobnost tkiva da se u njima izazove rast novih krvnih sudova.[8][11]
Postavlja se još jedno značajno pitanje je da li će neishemični miokard odgovoriti na stimulaciju faktorima rasta? Značajan broj podataka iz literature ukazuje da neishemična tkiva u velikoj meri reaguju na angiogenične stimulanse. To može da dovede ne tako često do nedostatka endogenog faktora rasta, ili da se promeni u ekstracelularnom matriksu, prisustvo inhibitora endogena, kao što su angiopoetin–2, i odsustvo ekspresije receptora faktora rasta i drugih signalizirajućih molekula koji su uključeni u angiogenetsku signalizaciju.[8]
Ovaj proces pored formiranja novostvorene mikrovaskulaturne mreže, uključuje i proliferaciju ćelija retinalnog pigmentnog epitela (RPE) zajedno sa inflamatornim ćelijama tipa neutrofila i makrofaga. Koncept horoidalna neovaskularizacije (CNV) i vaskularni aspekt procesa, su često udruženi sa apoptozom, endotelijalnom i inflamatornom infiltracijom, proliferacijom, remoduliranjem matriksa isl. Druga, nevaskularna komponenta koja vodi oštećenju makule oka i gubitku vida, je razvoj geografske atrofije retinalnog sloja i sloja RPE. Činjenica da se ovakva dva, bazično različita nalaza, udruženo razvijaju na istom oku, ukazuje na slične etiopatogenetske fenomene. U tom smislu, mnogobrojne studije usmerena ka definisanju uzroka bolesti, uz fiziološke procese starenja, ukazuju na povezanost eksudativne degeneracije makule sa pozitivnom porodičnom anamnezom, pušenjem cigareta, hipertenzijom, povišenim CRP, leukocitozom, navikama u ishrani, oksidativnim stresom, lokalnom ishemijom RPE i fotoreceptora…[12]


U kliničkom smislu, bitno je pratiti vidnu oštrinu i vidni komfor pacijenta (subjektivna metoda koja se izvodi pomoću optotipa i Amsler rešetkesa akcentom na centralni skotom i krivljenje slike ispred ispitivanog oka).
Od dodatnih dijagnostičkih metoda, poželjno je uraditi optičku koherentnu tomografiju (OCT) u smislu praćenja veličine eksudacije usamoj makuli. Ova metoda je senzitivnija u praćenju progresije bolesti od vidne funkcionalnosti, jer pacijent duže vreme nakon primene terapije ne primeti subjektivno poboljšanje dok se ono na OCT registruje već nakon nekoliko dana (iako je OCT još uvek samo pomoćna metoda u dijagnostici).[13]
Preporučen način lečenja je aplikacije anti-VEGF faktora (vascular endothelial growth factora, ili, slobodno prevodeći, vaskularnog endotelijalnog faktora rasta), intravitrealno (u staklasto telo oka), pod standardnim sterilnim uslovima i u ponovljenim dozama. Doza se ponavlja na četiri ili šest nedelja ili prema potrebi i kliničkoj slici.
Prema vodiču Evropskog udruženja retinologa, danas se za lečenje subfoealnih CNV koriste isključivo i samo anti-VEGF lekovi koji su prošli sveže ispitivanja, kao što su:
- Pegaptanib sodium (Macugen, Eyetech Pharmaceuticals, Inc-Pfizer Inc.)
Lek je odobren za upotrebu 2004. godine. To je aptamer sa specifičnim inhibicijom VEGF 165 izoformi. Bezbednost i efikasnost leka su potvrđeni: VISION (VEFG Inhibition Study in Ocular Neovascularisation) studijom.[14]
- Ranibizumab (Lucentis, Genentech, Inc-Novartis Pharma AG)
Lek je odobren za upotrebu juna 2006. godine. To je monoklonalno antitelo dobijeno fragmentacijom lanca bevacizumaba. Njegova efikasnost i bezebednost su potvrđeni: MARINA (Minimally/Classic Occult Trialod Anti-VEGF antibody ranibiyumab in the Treatment of Neovascular Age-related macular degeneration) studijom,[15] i ANCHOR (Anti-VEGF Antibody for the Treatmentof Predominantly Classic Choroidal Neovascularization inAMD ) studijom.[16]
- Bevacizubam (Avastin)
Ovaj lek, sa sličnim mehanizmom delovanja, kao prethodni, za nas u Srbiji je od posebnog interesa, jer je trenutno jedini lek iz grupe anti-VEGF faktora koji se može preporučiti pacijentima sa vlažnom makulopatijom (horoidalnom neovaskularizacijom u Srbiji.[17] Dosadašnje studije pokazalesu da je Avastin efikasan, bezbedan a veoma jeftin lek.[18][19][20][21][22][23]
Iako postoje pretpostavke da je lek retinalno toksična,[23][24] ima i istraživanja koja to opovrgavaju,[25][26][27] i zaključuju da doza bevacizumaba za intravitrealnu primenu do 2,5 mg nije toksična za retinu.[n 1]
Uz ipak preporučenu dozu za bezbednu intravitrealnu primenu, koja je nešto manja i iznosi 1—1,25 mg, potpuna stabilizacija barijere postiže se 28 dana nakon aplikacije anti VEGF leka[29]. Lek se već testiran i kod proliferative dijabetičke retinopatije,[29] rubeoze irisa i makularnog edema usled okluzije centralne retinalne vene.[30][31]
- ↑ Karen S. Moulton, Khashayar Vakili§, David Zurakowski, Mohsin Soliman, Catherine Butterfield, Erik Sylvin, Kin-Ming Lo, Inhibition of plaque neovascularization reduces macrophage accumulation and progression of advanced atherosclerosis pp. 4736–4741, PNAS April 15, (2003) vol. 100, no.8 [1] Pristupljeno 15.1.2014.
- ↑ Friedman D.S., O'Colmain B.J., Munoz B. et al.: Prevalence of age-related macular disease in the United States. Arch Ophthalmol 2004;122:564-72
- ↑ Chakravarthy U., Soubrane G., Bandell F. et al.: Evolving European guidance on the medical managment of neovascular age-related macular degeneratin. Br J Ophthalmol 2006; 90: 1188-1196.
- ↑ White F, Carroll S, Magnet A, et al. Coronary collateral development in swine after coronary arteryocclusion. Circ Res. 1992;71: 1490 –1500.
- ↑ Wolf C, Cai WJ, Vosschulte R, et al. Vascular remodeling and altered protein expression during growth of coronary collateral arteries. J Mol Cell Cardiol. 1998;30:2291–2305
- ↑ Gibson CM, Ryan K, Sparano A, et al. Angiographic methods to assess human coronary angiogenesis. Am Heart J. 1999;137:169 –179.
- ↑ Sasayama S, Fujita M. Recent insights into coronary collateral circulation. Circulation. 1992;85:1197–1204.
- ↑ 8,0 8,1 8,2 8,3 Seed & Walsh 2008: str. 90
- ↑ Ito W, Arras M, Scholz D, et al. Angiogenesis but not collateral growth is associated with ischemia after femoral artery occlusion. Am J Physiol. 1997;273:H1255–H1265.
- ↑ Li J, Post M, Volk R, et al. PR39, a peptide regulator of angiogenesis. Nat Med. 2000;6:49 –55.
- ↑ Jones MK, Wang H, Peskar BM, et al. Inhibition of angiogenesis by nonsteroidal anti-inflammatory drugs: insight into mechanisms and implications for cancer growth and ulcer healing [see comments]. Nat Med. 1999;5:1418 –1423
- ↑ Spaide R.F.: Aetilogy of Late Age-Related Macular Disease. In: Holz FG, Spaide RF. Medical Retina.Springer 2005:95- 129.
- ↑ Rosenfeld P.J., Moshfeghi A.A. and Puliafito C.A.: Optical coherence tomography findings after an intravitreal injection of bevacizumab (Avastin) for neovascular age-related macular degeneration.Ophthalmic Surg Lasers Imaging 2005; 36: 331-35.
- ↑ Gragoudas E.S., Adamis A.P., Cunningham E.T.Jr., Feinsod M., Guyer D.R.: VEGF Inhibition study in Ocular Neovascularization Clinical Trial Group. Pegaptanib for neovascular age-related macular degeneration. N. Engl. J. Med. 2004; 351: 2805-16
- ↑ Rosenfeld P.J., Brown D.M., Heler J.S., Boyer D.S., Kaiser P.K., Chung C.Y., Kim R.Y.: MARINA study group. Ranibizumab for neovascular age-related macular degeneration.N Engl J Med 2006:355:1419-31.
- ↑ Brown D.M., Kaiser P.K., Michels M., Soubrane G., Heier J.S., Kim R.Y., Sy J.P., Schneider S.: ANCHOR study group. Ranibizumab versus verteporfirin for neovascular agerelated macular degeneration. N Engl J Med 2006;355:1432-44
- ↑ Rosenfeld P.J.: Intravitreal Avastin: the low cost alternative to Lucentis? American Journal of Ophthalmology 2006; 142: 141-43.
- ↑ Stone E.M.: A very effective treatment for neovascular maculardegeneration. N Engl J Med 2006;355:1493-95.
- ↑ Rich R.M., Rosenfeld P.J., Puliafito C.A. et al.: Short-time safetyand efficacy of intravitreal bevacizumab (Avastin) forneovascular age-realted macular degeneration. Retina 2006;26(5): 495-511.(abstract)
- ↑ Spaide R.F., Laud K., Fine H.F. et al.: Intravitreal bevacizumabtreatment of choroidal neovascularization secondary toage-related macular degeneration.Retina 2006;26(4):383-90(abstract)
- ↑ Avery R.L., Pieramici D.J., Rabena M.D. et al.: IntravitrealBevacizumab (Avastin) for Neovascular age-related maculardegeneration. Ophthalmology 2006,113(3) 363.
- ↑ Bashshur Z.F., Bazarbachi A., Schakal A. et al.: IntravitrealBevacizumab for the management of choroidal neovascularisationin age-related macular degeneration. American Journalof Ophthalmology 2006;142(1):1-9.
- ↑ 23,0 23,1 Meyer C.H., Mennel S., Schmidt J.C., Kroll P.: Acute retinal pigment epithelial tear following intravitreal bevaciyumab (Avastin) injection for occult choroidal neovascularization secondary to age-related macular degeneration. Br J Ophthalmol 2006;90:1207-08.
- ↑ Lim J.I.: The pros and cons of bevacizumab therapy for subfoveal choroidal neovascularisation for age-related macular degeneration. Medscape Ophthalmology 2005;6(2) posted 12 /21/2005
- ↑ Manzano R.P.A., Peymen G.A., Khan Pet al.: Testing intravitrealtoxicity of bevacizumab (Avastin). Retina 2006; 26(3):257-61. (Abstract)
- ↑ Luthra S., Narayanan R., Marques L.E. et al.: Evaluation of invitro effects of bevacizumab (Avastin) on retinal pigment epithelial,neurosesory retinal and microvascular endothelialcells. Retina 2006;26(5):512-18.
- ↑ Spitzer M.S.,Wallenfels Thilo B., Sierra A. et al.: Antiproliferativeand cytotxic properties of bevacizumab on differentocular cells. Br J Ophthalmol 2006;90:1316-21.
- ↑ Bakri S.J., Cameron J.D., McCannel C.A. et al.: Abscence of histologic retinal toxicity of intravitreal bevacizumab in a rabbit model. American Journal of Ophthalmlogy 2006; 142(1) 162-64.
- ↑ 29,0 29,1 29,2 Ziemssen F., Neuhann I.M., Leitritz M. et al.: Does intravitreal injection of bevacizumab have an effect on the blood-aques barrier function? Br J Ophthalmol 2006;90:922
- ↑ Grisanti S., Biester S., Peters S. et al.: Intracameral Bevacizumabfor iris rubeosis. American Journal of Ophthalmology 2006;142 (1):158-60.
- ↑ Davidorf F.H., Mouser J.G., Derick R.J.: Rapid improvementof rubeosis iridis from a single bevacizumab (Avastin) injection.Retina 2006; 26(3):354-56.
