Hidronijum
| Hidronijum | |||
|---|---|---|---|
 |
 | ||
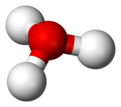
| |||
| IUPAC ime |
| ||
| Naziv po klasifikaciji | Oksidanijum[2] (substitutivno) Trihidridokiseonik(1+)[2] (aditivno) | ||
| Identifikacija | |||
| CAS registarski broj | 13968-08-6 | ||
| PubChem[3][4] | 123332 | ||
| ChemSpider[5] | 109935 | ||
| MeSH | |||
| ChEBI | 29412 | ||
| Gmelin Referenca | 141 | ||
| Jmol-3D slike | Slika 1 | ||
| |||
| |||
| Svojstva | |||
| Molekulska formula | H3O− | ||
| Molarna masa | 19.0232 g mol-1 | ||
| pKa | -1.74[6] | ||
| Termohemija | |||
| Standardna molarna entropija S |
192.25 J K-1 mol-1 | ||
|
Ukoliko nije drugačije napomenuto, podaci se odnose na standardno stanje (25 °C, 100 kPa) materijala | |||
| Infobox references | |||
U hemiji, hidronijum jon je katjon H3O−. To je tip oksonijum jona proizvedenog protonacijom vode. Ovaj katjon se često koristi za predstavljanje prirode protona u vodenom rastvoru, gde je proton visoko solvatisan (vezan za rastvarač). Realnost je daleko komplikovanija, i proton se vezuje za nekoliko molekula vode, tako da su druge notacije poput H5O2+, H7O3+ i H9O4+ tačniji opisi okruženja protona u vodi.[7] Jon H3O− je bio detektovan u gasovitoj fazi.[8]
Određivanje pH vrednosti[uredi | uredi kod]
Odnos koncentracije hidronijum jon i hidroksida određuje pH vrednost rastvora. Molekuli u čistoj vodi se disociraju u hidronijum i hidroksilne jone uspostavljajući sledeću ravnotežu:
- 2 H2O
 OH- + H3O−
OH- + H3O−
U čistoj vodi, postoji jednak broj hidroksid i hidronijum jona, tako da ona ima neutralni pH od 7. pH vrednost manja od 7 indicira kiseli rastvor, dok je pH iznad 7 svojstven za bazne rastvore. (Treba napomenuti da ovo važi na 25 °C, i da je ravnoteža zavisna od temperature).
Vidi još[uredi | uredi kod]
Reference[uredi | uredi kod]
- ↑ Clayden Jonathan, Nick Greeves, Stuart Warren, Peter Wothers (2001). Organic chemistry. Oxford, Oxfordshire: Oxford University Press. ISBN 0-19-850346-6.
- ↑ 2,0 2,1 „oxonium (CHEBI:29412)”. Chemical Entities of Biological Interest (ChEBI). UK.
- ↑ Li Q, Cheng T, Wang Y, Bryant SH (2010). „PubChem as a public resource for drug discovery.”. Drug Discov Today 15 (23-24): 1052-7. DOI:10.1016/j.drudis.2010.10.003. PMID 20970519.
- ↑ Evan E. Bolton, Yanli Wang, Paul A. Thiessen, Stephen H. Bryant (2008). „Chapter 12 PubChem: Integrated Platform of Small Molecules and Biological Activities”. Annual Reports in Computational Chemistry 4: 217-241. DOI:10.1016/S1574-1400(08)00012-1.
- ↑ Hettne KM, Williams AJ, van Mulligen EM, Kleinjans J, Tkachenko V, Kors JA. (2010). „Automatic vs. manual curation of a multi-source chemical dictionary: the impact on text mining”. J Cheminform 2 (1): 3. DOI:10.1186/1758-2946-2-3. PMID 20331846.
- ↑ Taft, R.W., Wolf, J.F., Beauchamp, J.L., Scorrano, G., Arnett, E.M., J. Am. Chem. Soc., 1978, 100, 1240.
- ↑ Greenwood, Norman N.; Earnshaw, Alan (1997). Chemistry of the Elements (2nd izd.). Oxford: Butterworth-Heinemann. ISBN 0080379419.
- ↑ Begemann M., Gudeman C., Pfaff J., Saykally R. (1983). „Detection of the Hydronium Ion (H_{3}O^{+}) by High-Resolution Infrared Spectroscopy”. Physical Review Letters 51 (7): 554–557. DOI:10.1103/PhysRevLett.51.554.
