Magnezijum karbonat – razlika između verzija
Prijeđi na navigaciju
Prijeđi na pretragu
Uklonjeni sadržaj Dodani sadržaj
m Bot: popravljanje preusmjeravanja |
m + |
||
| Red 1: | Red 1: | ||
{{Chembox-lat |
|||
{{Hemijsko jedinjenje |
|||
| Name = Magnezijum karbonat |
| Name = Magnezijum karbonat |
||
| ImageFile=Magnesium carbonate.png |
| ImageFile=Magnesium carbonate.png |
||
Verzija na datum 11 april 2014 u 07:30
| Magnezijum karbonat | |
|---|---|
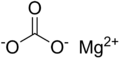
| |
| Drugi nazivi | Poznati su di-, tri- i penta-hidrat |
| Identifikacija | |
| CAS registarski broj | 546-93-0 |
| MeSH | |
| RTECS registarski broj toksičnosti | OM2470000 |
| Svojstva | |
| Molekulska formula | MgCO3 |
| Molarna masa | 84.32 g/mol |
| Agregatno stanje | bela čvrsta supstanca |
| Gustina | 2.958 g/cm3, osnovno |
| Tačka topljenja |
350 °C razlaže se |
| Rastvorljivost u vodi | 10.6 mg/100 ml |
| Struktura | |
| Kristalna rešetka/struktura | Romboedarska |
| Termohemija | |
| Standardna entalpija stvaranja jedinjenja ΔfH |
-1111.69 kJ/mol |
| Standardna molarna entropija S |
65.84 J.K−1.mol−1 |
| Srodna jedinjenja | |
| Drugi katjoni | Kalcijum-karbonat Stroncijum-karbonat Barijum-karbonat |
| Сродна једињења | artinit hidromagnezit dipingit |
|
| |
| Infobox references | |
Magnezijum karbonat, poznat i kao mineral magnezit kada je otkriven u prirodi, je hemijsko jedinjenje sa mnogo primena. Pri normalnim uslovima to je belo ili bezbojno hemijsko jedinjenje, male gustine, sa molekulskom formulom: MgCO3.[1][2] U hemiji se koristi za dobijanje magnezijum oksida, jer se na temperaturi preko 540 °C razlaže na magnezijum oksid i Ugljen dioksid. Magnezijum karbonat je magnezijumova so ugljene kiseline.
Reference
- ↑ Housecroft C. E., Sharpe A. G. (2008). Inorganic Chemistry (3rd izd.). Prentice Hall. ISBN 978-0-13-175553-6.
- ↑ Holleman A. F., Wiberg E. (2001). Inorganic Chemistry (1st edition izd.). San Diego: Academic Press. ISBN 0-12-352651-5.
