Fosfoenolpiruvatna kiselina
| Fosfoenolpiruvatna kiselina | |||
|---|---|---|---|

| |||
| IUPAC ime |
| ||
| Drugi nazivi | PEP | ||
| Identifikacija | |||
| CAS registarski broj | 138-08-9 | ||
| PubChem[1][2] | 1005 | ||
| ChemSpider[3] | 980 | ||
| DrugBank | DB01819 | ||
| ChEBI | 44897 | ||
| Jmol-3D slike | Slika 1 | ||
| |||
| |||
| Svojstva | |||
| Molekulska formula | C3H5O6P | ||
| Molarna masa | 168.04 g mol−1 | ||
|
Ukoliko nije drugačije napomenuto, podaci se odnose na standardno stanje (25 °C, 100 kPa) materijala | |||
| Infobox references | |||
Fosfoenolpiruvatna kiselina (PEP, fosfoenolpiruvat) je anjon koji je značajno hemijsko jedinjenje u biohemiji. Ona sadrži visokoenergijske fosfatne veze (-61,9 kJ/mol), i učestvuje u glikolizi i glukoneogenezi. Kod biljki, ona takođe učestvuje u biosintezi raznih aromatičnih jedinjenja i u fiksaciji ugljenika, dok se kod bakterija koristi kao izvor energije za fosfotransferazni sistem.
U glikolizi[uredi | uredi kod]
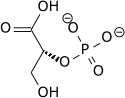
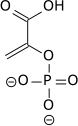
PEP se formira dejstvom enzima enolaza na 2-fosfoglicerat. Metabolizam PEP-a do piruvata posredstvom piruvatne kinaze (PK) formira se 1 molekul adenozin trifosfata (ATP) putem fosforilacije supstrata. ATP je jedan od glavnih nosilaca hemijske energije u ćelijama.
| 2-fosfo{small|D}glicerat | Enolaza | fosfoenolpiruvat | Piruvatna kinaza | piruvat | ||
|
|

| ||||
| H2O | ADP | ATP | ||||
|

| |||||
| H2O | ||||||
| Enolaza | Piruvatna kinaza | |||||
Jedinjenje C00631 u KEGG bazi podataka metaboličkig puteva. Enzim 4.2.1.11 u KEGG bazi podataka metaboličkig puteva. Jedinjenje C00074 u KEGG bazi podataka metaboličkig puteva. Enzim 2.7.1.40 u KEGG bazi podataka metaboličkig puteva. Jedinjenje C00022 u KEGG bazi podataka metaboličkig puteva.
U glukoneogenezi[uredi | uredi kod]
PEP se formira dekarboksilacijom oksaloacetata i hidrolizom jednog molekula guanozin trifosfata. Ta reakcija je katalizovana enzimom fosfoenolpiruvat karboksikinaza (PEPCK), i ona je korak koji ograničava brzinu glukoneogeneze:[4]
- GTP + oksaloacetat → GDP + fosfoenolpiruvat + CO2
U biljkama[uredi | uredi kod]
PEP se koristi u sintezi horizmata u putu šikimata.[5] Horiumat zatim može da bude metabolisan u aromatične aminokiseline (fenilalanin, triptofan i tirozin) i druga aromatična jedinjenja.
Osim toga, kod C4 biljki, PEP služi kao važan supstrat u fiksaciji ugljenika. Hemijska reakcija je katalizovana fosfoenolpiruvat karboksilazom (PEP karboksilaza):
- PEP + HCO3- → oksaloacetat
Reference[uredi | uredi kod]
- ↑ Li Q, Cheng T, Wang Y, Bryant SH (2010). „PubChem as a public resource for drug discovery.”. Drug Discov Today 15 (23-24): 1052-7. DOI:10.1016/j.drudis.2010.10.003. PMID 20970519.
- ↑ Evan E. Bolton, Yanli Wang, Paul A. Thiessen, Stephen H. Bryant (2008). „Chapter 12 PubChem: Integrated Platform of Small Molecules and Biological Activities”. Annual Reports in Computational Chemistry 4: 217-241. DOI:10.1016/S1574-1400(08)00012-1.
- ↑ Hettne KM, Williams AJ, van Mulligen EM, Kleinjans J, Tkachenko V, Kors JA. (2010). „Automatic vs. manual curation of a multi-source chemical dictionary: the impact on text mining”. J Cheminform 2 (1): 3. DOI:10.1186/1758-2946-2-3. PMID 20331846.
- ↑ „InterPro: IPR008209 Phosphoenolpyruvate carboxykinase, GTP-utilising”. Pristupljeno 17. 08. 2007.
- ↑ „BioCarta - Charting Pathways of Life”. Pristupljeno 17. 08. 2007.
