Di(fenil)-(2,4,6-trinitrofenil)iminoazanijum
| Di(fenil)-(2,4,6-trinitrofenil)iminoazanijum | |||
|---|---|---|---|

| |||
| IUPAC ime |
| ||
| Drugi nazivi | 2,2-difenil-1-pikrilhidrazil 1,1-difenil-2-pikrilhidrazil radikal 2,2-difenil-1-(2,4,6-trinitrofenil)hidrazil Difenilpikrilhidrazil | ||
| Identifikacija | |||
| Abrevijacija | DPPH | ||
| CAS registarski broj | 1898-66-4 | ||
| PubChem[1][2] | 74358 | ||
| ChemSpider[3] | 2016757 | ||
| Jmol-3D slike | Slika 1 | ||
| |||
| |||
| Svojstva | |||
| Molekulska formula | C18H12N5O6 | ||
| Molarna masa | 394.32 g/mol | ||
| Agregatno stanje | Prah nijansi od crne do zelene, ljubičasti rastvor | ||
| Gustina | 1.4 g/cm3 | ||
| Tačka topljenja |
135 °C, 408 K, 275 °F (razlaže se) | ||
| Rastvorljivost u vodi | nerastvorljiv | ||
| Opasnost | |||
| Podaci o bezbednosti prilikom rukovanja (MSDS) | MSDS | ||
| NFPA 704 | |||
|
Ukoliko nije drugačije napomenuto, podaci se odnose na standardno stanje (25 °C, 100 kPa) materijala | |||
| Infobox references | |||
DPPH je česta skraćenica za organsko jedinjenje 2,2-difenil-1-pikrilhidrazil. Predstavlja tamni kristalasti prah koga čine stabilni slobodni radikali. DPPH ima dve bitne primene: praćenje hemijskih reakcija slobodnih radikala i standard pozicije i intenziteta ESR signala.
Svojstva i primena[uredi | uredi kod]
DPPH ima nekoliko kristalnih formi koje se razlikuju po simetriji kristalne rešetke i po tački topljenja. Komercijalni prah je mešavina faza koja se topi na oko 130 °C. DPPH-I (t. t. 106 °C) je ortorombičan, DPPH-II (t. t. 137 °C) je amorfan i DPPH-III (t. t. 128–129 °C) je trikliničan.[4]
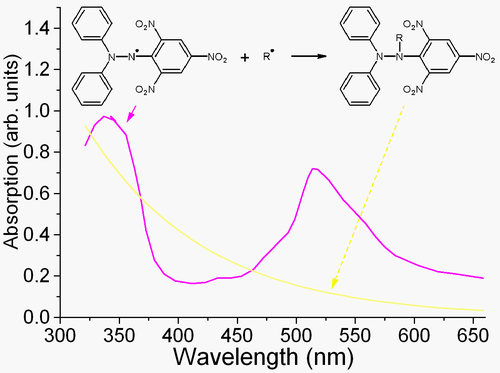
DPPH je poznata zamka ("hvatač", jez-eng|scavenger) za druge radikale. Stoga, brzina redukcije pri hemijskoj reakciji u kojoj učestvuje DPPH predstavlja meru radikalske prirode te reakcije. Zbog oštrog pika apsorpcije na 520 nm, DPPH radikal ima tamno-ljubičastu boju u rastvoru, a postaje bezbojan ili žut kada se redukuje (neutralizuje). Ovo svojstvo omogućava vizuelno praćenje reakcije, a broj radikala na početku može se utvrditi po promeni apsorbance na 520 nm ili po ESR signalu DPPH radikala.[5]
Zato što je hvatač radikala, on je jak inhibitor polimerizacije slobodnoradikalskog mehanizma.[6]

Kao stabilan i dobro karakterizovan čvrst izvor radikala, DPPH je tradicionalan i možda najpopularniji standard (g-faktor) za poziciju i intenzitet ESR signala - broj radikala u sveže pripremljenom uzorku može se odrediti merenjem težine i ESR faktor cepanja za DPPH kalibrisan na g = 2.0036. DPPH signal je pogodan jer je obično koncentrisan samo u jednoj liniji, čiji intenzitet se povećava linearno sa kvadratnim korenom mikrotalasne snage u širem opsegu. Razređena priroda DPPH radikala (jedan nesparen elektron na 41 atom) daje relativno malu širinu spektralne linije (1.5–4.7 Gausa). Međutim, širina linije se povećava ako molekuli rastvarača ostanu u kristalu i ako su merenja rađena na visokim frekvencijama (~200 GHz), gde mala g-anizotropija DPPH radikala postaje primetna.[7][8]
Iako je DPPH pri normalnim uslovima paramagnetična čvrsta supstanca, prelazi u antiferomagnetično stanje pri hlađenju na izuzetno niske temperature reda 0.3 K. Ovaj fenomen je prvi put uočio Aleksandar Mihajlovič Prohorov 1963. godine.[9][10][11][12]
Reference[uredi | uredi kod]
- ↑ Li Q, Cheng T, Wang Y, Bryant SH (2010). „PubChem as a public resource for drug discovery.”. Drug Discov Today 15 (23-24): 1052-7. DOI:10.1016/j.drudis.2010.10.003. PMID 20970519.
- ↑ Evan E. Bolton, Yanli Wang, Paul A. Thiessen, Stephen H. Bryant (2008). „Chapter 12 PubChem: Integrated Platform of Small Molecules and Biological Activities”. Annual Reports in Computational Chemistry 4: 217-241. DOI:10.1016/S1574-1400(08)00012-1.
- ↑ Hettne KM, Williams AJ, van Mulligen EM, Kleinjans J, Tkachenko V, Kors JA. (2010). „Automatic vs. manual curation of a multi-source chemical dictionary: the impact on text mining”. J Cheminform 2 (1): 3. DOI:10.1186/1758-2946-2-3. PMID 20331846.
- ↑ Kiers C. T., De Boer J. L., Olthof R., Spek A. L. (1976). „The crystal structure of a 2,2-diphenyl-1-picrylhydrazyl (DPPH) modification”. Acta Crystallographica Section B Structural Crystallography and Crystal Chemistry 32: 2297. DOI:10.1107/S0567740876007632.
- ↑ Mark S. M. Alger (1997). Polymer science dictionary. Springer. str. 152. ISBN 0412608707.
- ↑ Cowie J. M. G., Arrighi Valeria (2008). Polymers: Chemistry and Physics of Modern Materials (3rd izd.). Scotland: CRC Press. ISBN 0-8493-9813-4.
- ↑ M.J. Davies (2000). Electron Paramagnetic Resonance. Royal Society of Chemistry. str. 178. ISBN 0854043101.
- ↑ Poole, Charles P. (1996). Electron spin resonance: a comprehensive treatise on experimental techniques. Courier Dover Publications. str. 443. ISBN 0486694445.
- ↑ A. M. Prokhorov and V.B. Fedorov, Soviet Phys. JETP 16 (1963) 1489.
- ↑ Teruaki Fujito (1981). „Magnetic Interaction in Solvent-free DPPH and DPPH–Solvent Complexes”. Bulletin of the Chemical Society of Japan 54 (10): 3110.
- ↑ Stig Lundqvist (1998). „A. M. Prokhorov”. Nobel lectures in physics, 1963-1970. World Scientific. str. 118. ISBN 981023404X.
- ↑ Aleksandr M. Prokhorov, The Nobel Prize in Physics 1964
Literatura[uredi | uredi kod]
- Poole, Charles P. (1996). Electron spin resonance: a comprehensive treatise on experimental techniques. Courier Dover Publications. str. 443. ISBN 0486694445.
- Stig Lundqvist (1998). „A. M. Prokhorov”. Nobel lectures in physics, 1963-1970. World Scientific. str. 118. ISBN 981023404X.
- M.J. Davies (2000). Electron Paramagnetic Resonance. Royal Society of Chemistry. str. 178. ISBN 0854043101.
- Cowie J. M. G., Arrighi Valeria (2008). Polymers: Chemistry and Physics of Modern Materials (3rd izd.). Scotland: CRC Press. ISBN 0-8493-9813-4.
- Mark S. M. Alger (1997). Polymer science dictionary. Springer. str. 152. ISBN 0412608707.