Ureja
| Ureja | |||
|---|---|---|---|
| |||
 |
 | ||
| IUPAC ime |
| ||
| Drugi nazivi | Karbamid, karbonil diamid, karbonildiamin, diaminometanal, diaminometanon | ||
| Identifikacija | |||
| CAS registarski broj | 57-13-6 | ||
| PubChem[1][2] | 1176 | ||
| ChemSpider[3] | 1143 | ||
| UNII | 8W8T17847W | ||
| KEGG[4] | |||
| ChEMBL[5] | CHEMBL985 | ||
| RTECS registarski broj toksičnosti | YR6250000 | ||
| Jmol-3D slike | Slika 1 | ||
| |||
| |||
| Svojstva | |||
| Molekulska formula | CH4N2O | ||
| Molarna masa | 60.06 g mol−1 | ||
| Agregatno stanje | bela čvrsta materija | ||
| Gustina | 1.32 g/cm3 | ||
| Tačka topljenja |
133–135 °C | ||
| Rastvorljivost u vodi | 107,9 g/100 ml (20 °C) 167 g/100ml (40 °C) 251 g/100 ml (60 °C) 400 g/100 ml (80 °C) | ||
| Baznost (pKb) | pKBH+ = 0.18[6] | ||
| Struktura | |||
| Dipolni moment | 4.56 D | ||
| Opasnost | |||
| Podaci o bezbednosti prilikom rukovanja (MSDS) | JT Baker | ||
| EU-indeks | nije na listi | ||
| Tačka paljenja | nije zapaljiva | ||
| Srodna jedinjenja | |||
| Srodna uree | Tiourea Hidroksikarbamid | ||
| Srodna jedinjenja | Karbamid peroksid Urea fosfat | ||
|
Ukoliko nije drugačije napomenuto, podaci se odnose na standardno stanje (25 °C, 100 kPa) materijala | |||
| Infobox references | |||
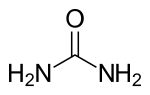
Ureja ili karbamid je organski spoj hemijske formule (NH2)2CO. Ureju je otkrio 1773. godine francuski hemičar Hilaire Rouelle, u urinu. Urea je prvi organski spoj sintetiziran iz anorganskih spojeva, što je uspjelo 1828. godine Friedrich Wöhleru:[7]
Urea igra glavnu ulogu u metabolizmu azotnih spojeva kod životinja i ljudi i glavna je supstanca koja sadrži azot u mokraći.
Urea nastaje u procesu razgradnje proteina u jetri u ciklusu ureje. Organizam sintetizira ureju iz amonijaka, produkta razgradnje proteina.[8][9]
Urea se za komercijalnu primjenu sintetizira iz amonijaka i ugljen dioksida. Više od 90% svjetske proizvodnje se koristi u poljoprivredi kao umjetno gnojivo.
Dobivanje[uredi | uredi kod]

Prije razvoja tehničkih metoda sinteze i njene upotrebe, koji je uslijedio u novije vrijeme, urea je bila zanimljiva prvenstveno zbog toga što je ona glavni konačni produkt metabolizma dušika u sisavaca i izlučuje se u urinu.
Ureu je 1773.g. francuska kemičarka Hilaire Rouelle izolirala iz urina, premda nije bila sve do 1799. potpuno karakterizirana niti imenovana ureom, kada je pobliže ispitana i određena su joj fizikalna svojstva. Prvi ju je vjerojatno sintezirao John Davy, brat Sir Humphrey Davya. On je 1811.g. načinio fozgen djelovanjem sunčanog svjetla na smjesu klora i ugljikova monoksida, a 1812.g. objavio da dobiveni produkt reakcijom sa suhim amonijakom daje krutu tvar, koja ne razvija ugljikov dioksid kad se na nju djeluje octenom kiselinom, pa prema tome nije amonijev karbonat. Svoj produkt Davy nije identificirao kao ureu, pa je zasluga za sintezu uree pripala Friedrich Wöhleru, koji je 1828.g. opazio da je produkt dobiven kuhanjem otopine amonijeva cijanata s vodom identičan s ureom izoliranom iz urina.
Urea je prva organska tvar (prvi sintetizirani organski spoj) dobivena sintezom od anorganskih tvari/spoja (amonijeva cijanata); tom je sintezom njemački kemičar F. Wohler 1828.g. pobio dotadašnje mišljenje i vitalističku teoriju da organski spojevi mogu nastati samo od organizama (i u živim stanicama organizama) pod utjecajem i djelovanjem „životne sile“ i time utro put razvoju organske kemije.
Urea se za komercijalnu primjenu sintetizira zagrijavanjem smjese amonijaka i ugljikovog dioksida pod tlakom. Godišnje se proizvede nekoliko 100,000,000 tona ureje.
Uporaba[uredi | uredi kod]
Industrijski se proizvodi u velikim količinama, a rabi se ponajprije kao koncentrirano umjetno dušično gnojivo (najčešće 46% vezanog dušika), koje biljke lako asimiliraju. Više od 90% svjetske proizvodnje se koristi u poljoprivredi kao umjetno gnojivo.
Osim toga, služi kao jeftin izvor dušika u hranidbenim podlogama za industrijske mikrobne procese, za proizvodnju melamina, umjetnih smola (ureaformaldehidne smole), polimernih materijala (aminoplasti), ljepila, u manjoj mjeri lijekova i eksploziva te u kozmetici.
Reference[uredi | uredi kod]
- ↑ Li Q, Cheng T, Wang Y, Bryant SH (2010). „PubChem as a public resource for drug discovery.”. Drug Discov Today 15 (23-24): 1052-7. DOI:10.1016/j.drudis.2010.10.003. PMID 20970519.
- ↑ Evan E. Bolton, Yanli Wang, Paul A. Thiessen, Stephen H. Bryant (2008). „Chapter 12 PubChem: Integrated Platform of Small Molecules and Biological Activities”. Annual Reports in Computational Chemistry 4: 217-241. DOI:10.1016/S1574-1400(08)00012-1.
- ↑ Hettne KM, Williams AJ, van Mulligen EM, Kleinjans J, Tkachenko V, Kors JA. (2010). „Automatic vs. manual curation of a multi-source chemical dictionary: the impact on text mining”. J Cheminform 2 (1): 3. DOI:10.1186/1758-2946-2-3. PMID 20331846.
- ↑ Joanne Wixon, Douglas Kell (2000). „Website Review: The Kyoto Encyclopedia of Genes and Genomes — KEGG”. Yeast 17 (1): 48–55. DOI:10.1002/(SICI)1097-0061(200004)17:1<48::AID-YEA2>3.0.CO;2-H.
- ↑ Gaulton A, Bellis LJ, Bento AP, Chambers J, Davies M, Hersey A, Light Y, McGlinchey S, Michalovich D, Al-Lazikani B, Overington JP. (2012). „ChEMBL: a large-scale bioactivity database for drug discovery”. Nucleic Acids Res 40 (Database issue): D1100-7. DOI:10.1093/nar/gkr777. PMID 21948594.
- ↑ Williams, R. (24. 10. 2001.). „pKa Data”. Arhivirano iz originala na datum 2003-08-24. Pristupljeno 27. 11. 2009.
- ↑ Tehnički leksikon, Leksikografski zavod Miroslav Krleža; glavni urednik: Zvonimir Jakobović. Tiskanje dovršeno 21. prosinca 2007.g., Nacionalne i sveučilišne knjižnice u Zagrebu pod brojem 653717. ISBN 978-953-268-004-1, str. 931.
- ↑ Clayden Jonathan, Nick Greeves, Stuart Warren, Peter Wothers (2001). Organic chemistry. Oxford, Oxfordshire: Oxford University Press. ISBN 0-19-850346-6.
- ↑ Susan Budavari, ur. (2001). The Merck Index: An Encyclopedia of Chemicals, Drugs, and Biologicals (13th izd.). Merck Publishing. ISBN 0-911910-13-1.

