Kolateralna cirkulacija
| Колатерална циркулација | |
|---|---|
| Klasifikacija i eksterni resursi | |
| ICD-10 | I20-I25 |
| ICD-9 | 410-414, 429.2 |
| MedlinePlus | 007115 |
| eMedicine | radio/192 |
| MeSH | D003324 |
Kolateralna cirkulacija je mreža tankih krvnih sudova koja u normalnim uslovima ili nerazvijenom obliku nije otvorena. Kada se arterije suze do nivoa u kome je protok krvi kroz određno tkivo limitirano ili ograničeno (koronarna bolest srca [1], okluzija arterija nogu itd.), kolateralna cirkulacija može postane aktivna i uvećana. To omogućava protok krvi, zaobilaznim pravcima, oko blokirane (sužene) arterije, do obližnje arterije ili do iste arterije ispod mesta suženja. Na taj način kolaterale štite ugroženo tkivo ili organ od oštećenja.[2][3][4][5][6]
Stanje i aktivnost kolateralni cirkulacije može značajno uticati na kliničku sliku, tok bolesti, komplikacije i samim tim na prognozu bolesti i bolesnika. Na osnovu iznetog proističe zaključak o velikom značaju kolateralne cirkulacij, koja može da smanji ne samo obim i stepen ishemije, već i veličinu zone lezije (infarkt) ili čak spreči njen razvoj. Broj, raspored i protok kroz kolateralni krvotom dijagnostički se lako može utvrditi arterioografijom, i može biti od značaja za izbor oblika i načina lečenja.[7]
Savremena terminologija[uredi | uredi kod]
Pojam kolateralna cirkulacija ne treba mešati sa pojmovima; vaskulogeneza, angiogeneza, arteriogeneza koji se koriste za opisivanje procesa formiranje novih krvnih sudova (neovaskularizacija),[8][9][10][11][12] jer pojam kolateralna cirkulacija označava već postojeću cirkulaciju koja je u organizmu u normalnom stanju u nerazvijenom obliku.[2]
- Vaskulogeneza, je embrionalna neovaskularizacija i odnosi se na formiranje primitivnih (prvobitnih) krvnih sudova unutar ploda i njegove okolne membrane i uključuje „in situ“ diferencijaciju iz mezoderma izvedenih angioblasta, koji se gomilaju i formaju nove krvne sudove.
- Angiogeneza podrazumeva formiranje novih krvnih sudova preko klijanja ili odvajanja od već postojećih krvnih sudova i javlja se kako pre tako i postnatalno. Vaskularizacija mozga nastaje prvenstveno kroz angiogenezu.
- Arteriogeneza, označava proces širenja kolaterala iz već postojećih arteriola, od kojih se formiraju veće arterije. Ona se definiše i kao proces formiranja krvnog suda iz vaskularnog zida koji se sastoji od intime, medije i adventitcije.
- Anastomoza krvnih sudova, je prirodno ili veštački stvorena kolateralna veza između krvnih sudova, koja omogućava preusmeravanje tok krvi kod postojanja barijere u nekom krvnom sistemu. Arterijske anastomoze, poput onih u mozgu, rukama, ili u stomaku omogućavajući adekvatan protok krvi u nekim od začepljenih krvnih sudova. Veštačko anastomoze je hiruška metoda, koja ima za cilj poboljšanje snabdevanje krvlju tkiva u nekim vaskularnim bolestima.[13]
Istorijat[uredi | uredi kod]
Funkcionalni značaj kolateralnih krvnih sudova pozat je više od tri veka. Prvi put dokumentovano je njihovo postajanje kod čoveka i živtinja pre sedam decenija. Sadašnji koncept razvoja kolateralne cirkulacije baziran je na anatomskim studijama, čije rezultate su prvi prikazali 1961. godine DŽejms (James),[14], Baroldi (Baroldi),[15] i Skomazoni (Scomazzoni) koji su kolateralne krvne sudove na srcu klasifikovali kao homokoronarne (jer povezuju segmente iste arterije) i interkoronarne (jer povezuju segmente različitih arterija).
Nakon serija eksperimenata Šepar [16] je u kasnim šezdesetim i sedamdesetim godinama 20. veka proširio stanja o mehanizmima, po kojima se ovi krvni sudovi (obično van funkcije), mikroskopskih veličina (40-10 milimikrona u prečniku u svom prirodnom stanju),[17] transformišu u ishemiji ili stenozi u krvne sudove značajne veličine i funkcije za očivanje protoka krvi a često i života. Ova saznanja nastala su, uprkos brojnim studijama koje su negirale funkciju kolateralnih krvnih sudova u spasavanju ugrožene perfuzije tkiva u ishemiji i očuvanje krvnog pritiska.[18]
Tokom 1980-ih postignut je konsenzus među istraživačima da ovi krvni sudovi mogu da sačuvaju 30 do 40% koronarnog protoka krvi kod delimičnog začepljenja krvnih sudova srca , spreče ishemiju i sčani udar.[19]
Anatomsko-patofiziološke karakteristike kolateralne cirkulacije[uredi | uredi kod]
Kolaterale su vaskularni kanali tankog zida, malog dijametra (od 20 do 200 mikrona) koji u pojedinim organima postoje u nerazvijenom i nefunkcionalnom obliku ili se u određenim stanjima mogu naknadno formirati. Kolateralni krvni sudova su u normalnom uslovima zatvoreni i nefunkcionalni, zato što između njihovih krajnjih tačaka ne postoji gradijent pritiska. koji bi kroz njih pokretao protok krvi između arterija koje povezuju.[20]
„Made se kolaterale mogu naći na obdukciji one se ne mogu prikazati na angiografiji u normalnoj ili lako oštećenoj cirkulaciji, jer nose minimalni protok i njihova veličina je ispod granice rezolucije sadašnjih prikazivača slike koronografijom“[2].
Tek u prisustvu kritične lezije ili okluzije oni postaju funkcionalni. U hipoksičnim uslovima, kada stenoza krvnog suda mora biti barem 70%, pod uticajem gradijenta pritiska i adenozina, dolazi do aktivinja kolaterala i razvoja angiogeneze koja je, pod uticajem endotelnog faktora rasta. U tim uslovima dolazi do otvaranja kolateralnog krvotoka i uspostavljanja protoka krvi u ugroženom organu.[20]
Transformacija postojećih nefunkcionalnih kolaterala u „zrele“, razvijene kolaterala naziva se arteriogeneza. Za razliku od arteriogeneze koja podrazumeva formiranje razvijene kolateralne mreže od već postojećih nerazvijenih, nefunkcionalnih, rudimentalnih kolaterala, angiogeneza podrazumeva razvoj novih krvnih sudova od već postojećih i obično rezultuje formiranjem malih kapilara slične strukture.[n 1] Brzina i stepen njihovog nastajanja zavisi od stepena stenoze (suženja) i vremena izloženosti tkiva ishemiji. Razvoj kolateralnih krvnih sudova verovatno je genetski predisponiran.[21]
Zahvaljujući uspostavljanju protoka kroz kolaterle, iste promene u angiogramu velikih krvnih sudova ne daju isti elektrokardiografski nalaz i kliničku sliku. Dobro razvijena kolateralna cirkulacija sprečava nastajanje nekroze i uništavanja kolagena posle infarktin stanja i često spasava život. Zato su kolateralni krvni sudovi jako bitni u prognozi koronarne bolesti, infarkta miokarda i periferne arterijske bolesti, naročito u periodu pre bilo koje intervencije.[21]
Kolaterale u fiziološkim stanjima[uredi | uredi kod]
Za razliku od venskih anastomoza, koji su brojnije i značajnije, često sa unutrašnjim prečnikom od 1 do 2 mm, arterijske kolaterale su npr u zdravom ljudskom srcu, unutrašnjeg prečnika oko 40 mikrona.[21] U preliminarnim studijama utvrđeno je da fiziološke kolaterale mogu takođe biti prčnika 100 mikrona, ili više.[22] U fiziološkim stanjima kretanje krvi kroz kolaterale je beznačajna zbog nedovoljne razlike u pritisku. Zato se često ovi krvni sudovi nazivaju „uspavani kolaterali“.
Razne životinjske vrste značajno se razlikuju po broju, izgledu i rasporedu kolaterala. Takođe i među ljudskih bićima, u fiziološkim stanjima, postoje velike razlike u broj i rasporedu kolaterala. Razlike su posebno izražene na prednjoj i zadnjoj strani srca, kao i u oblasti atrijalnog i interventrikularnog septuma. Među najznačajnije kolaterale srca spadaju one koje pripadaju epikardijumu, i koje se pružaju po površini obe komore i spajaju sve tri glavne koronarne arterije .
Kolaterale u patološkim stanjima[uredi | uredi kod]
U patološkim stanjima kolateralna cirkulacija ima veliki značaj, jer bolesniku može spasiti život, sprečiti nastanak srcanog udara i poboljšati kvalitet života. Za razvoj kolateralne cirkulacije koja zadržava trajnu protočnu sposobnost u pojedinim stanjima, potrebno je da prođe nekoliko nedelja, meseci ili cela godina.
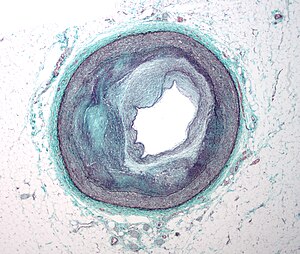
Kolaterale se aktiviraju ili nastaju i u patološkim stanjima, kada zbog značajnog suženja ili začepljenja, zahvaćeni krvni sud predstavlja barijeru i utiče na promenu pritiska (poststenotični pritiska) u područjima koji on vaskularizuje, zbog čega pritisak značajno opada. Niske vrednosti pritiska npr u bolesnika sa okluzijom srčanih arterija rezultuje aktivacijom kolaterala koje povezuju normalne i bolesne srčane arterije, kako bi kompenzovale nastalu razliku pritiska. Razlika pritiska je ta koja pokreće cirkulaciju krvi kroz kolaterale. Pod dejstvom pritiska, koji je iznad normalnog, otvara se kolateralna cirkulacija što omogućava protok krvi, čime se kompenzuje niska vrednost pritiska izazvana značajnim suženjem ili začepnjenjm obolelih krvnih sudova. Stres krvnih sudova i vazodilatacija, koji se aktiviraju u obolelom području na nastalu ishemiju u tkivu, podstiču ne samo širenje postojećih krvnih sudova već i stvaranje novih. Protočnaa sposobnost kolateralne cirkulacije nije velika. Prorocenjuje da dobro razvijena kolateralna cirkulacija kod suženih koronarnih arterija može dati takav protok krvi, koji anterogradno iznosi i do 90% protoka u odnosu na suženi prečnik krvnog suda.[23] Uprkos očigledno niskom protoku, zbog svojih ograničenih mogućnosti ipak kolaterale imaju veliki klinički značaj.
Najjači stimulusi za arteriogeni proces u kolateralnoj cirkulaciji u patološkim stanjima su;
- konstrikcija začepljene arterije (kao primarni faktor) koja dovodi do transanastomotičkog gradijent pritiska,
- veličina i stanje lumena distalnog dela kolaterala,
- vaskularni otpor (npr. otpor koronarnih krvnih sudova),
- viskoznost krvi
- kontraktilnost mišića (npr. srčanog mišića),
- fizička aktivnost bolesnika,
- hiperholestrolemija.
Kolateralna cirkulacija i njen značaj[uredi | uredi kod]

Kolateralna cirkulacija je mreža tankih krvnih sudova koja u normalnim uslovima nije otvorena. Kada se arterije suze do tačke kada je protok krvi kroz određno tkivo limitirano (koronarna bolest srca, okluzija arterija nogu itd.), kolateralna cirkulacija može da se uveća i postane aktivna. To omogućava protok krvi oko blokirane (sužene) arterije do obližnje arterije ili do iste arterije ispod mesta suženja, štiteći tkivo od oštećenja. Zato se smatra da je jedan od oblika dugoročne regulacije protoka krvi razvoj kolateralne cirkulacije nakon prekida dotoka krvi u nekom tkivu.[24]
Dugoročno povećanje protoka krvi kroz kolaterale je posledica značajnog anatomskog povećanja kolateralnih krvnih sudova, čiji ukupni zbir poprečnih preseka može biti često veća od presaka začepljene arterije. Brzina nastanka okluzije (začepljenja) nekog krvnog suda od izuzetnog je značaja za razvoj kolateralne cirkulacije. Tako npr kod postepenog sužavanja koronarnih arterija nastaju kolaterale većeg prečnika sa većom protočnom sposobnošću. To omogućava srcu da vrlo brzo podesi svoju radnu sposobnost sniženom nivou koronarnog protoka.[25][26] Ovim promenama u kolateralnoj cirkulaciji može se objasniti zašto se i pri potpunom začepljenom koronarnih artrije ne javljaju klinički znaci infarkta., iako se u kasnijem periodu u takvom srčanom mišiću mogu javiti manifestni oblici hronične ishemije, uglavnom posle napora. Za takve pacijente je karakteristično da i pored okluzije koronarne arterije zbog dobre kolateralizacije imaju manje izražene stenokardične tegobe, ali sa niskom verovatnoćom za srčani udar (infarkt). Ovakvo stanje se obično sreće kod osobe koje su fizički aktivne, jer imaju dobro razvijenu kolateralnu cirkulaciju, što smanjuje učestalost infarkta srca.[27]
Značaj kolateralne cirkulacije može se sagledati i na primeru začepljenja butne arterije noge, kada mali krvni sudovi koji mimoilaza okluziju (butne arterije), mogu toliko da se prošire i skoro potpuno (kod mlađih ljudi) obezbede odgovarajuće snadevanje krvlju, što se odvija kroz više faza;[28]
- Odmah nakon začepljenja zbog nedovoljne razvijensoti kolaterala, protok krvi pada na svega 3/8 normalnog protoka.
- Nakon nekoliko minuta protok krvi se vraća na 1/2 normalne vrednosti.
- U daljem periodu od jednog ili više dana protok krvi će se vratiti na normalu, što je praćeno i sve većim uvećanjem promera kolateralnih krvnih sudova.
Akutno aktiviranje (otvaranje) kolateralnih krvnih sudova mogu pored vaskularnih (okluzivnih) izazvati i metabolički faktori i snižavanje arterijskog krvnog pritiska zbog smanjenog priliva krvi i hranljivih materija u ugroženom tkivu.
Dobro razvijena kolateralna cirkulacija igra značajnu ulogu u smanjenju vaskularnog rizika nakon subokluzije ili okluzije krvnih sudova u okluzivnoj bolesti. Prisustvo dobro razvijene kolateralne cirkulacije npr. signifikantno smanjuje rizik od nastabilnih koronarnih događaja;[29]
- U jednoj studiji od 403 pacijenata sa stabilnom anginom pektoris smrtni ishod nakon akutnog infarkta miokarda registrovan je u 2,2% pacijenata sa dobrom kolateralnom cirkulacijom, u odnosu na pacijente sa lošom kolateralnom cirkulacijom kod kojih je procenat smrtnosti bio 9%.[30]
- Incidencija stabilne angine pektoris u odnosu na nestabilnu je značajno veća kod pacijenata sa dobrom kolateralnom cirkulacijom u odnosu na ona sa lošom (21% : 12%).[2]
Kolateralna cirkulacija u prevenciji i terapiji[uredi | uredi kod]
Mada se sposobnost pojedinaca da razviju kolateralnu cirkulaciju često zanemaruje, ipak treba imati u vidu da je ona potencijalno od velikog značaja, u odlučujućim trenucima ishemije, kao zaštita od teških posledica pa i gubitka života. Dobro razvijeni koronarni kolaterali mogu pomoći u zaštiti srčanog mišića od srčanog udara tokom epizode ishemije, ali i da produže trajanje ograničenog i dragocenog vremena, tzv „zlatnog standarda“ koji vremeski traje od početka akutnog srčanog udara, do uspešne koronarne reperfuzije srčanog mišića.
Osnovne postavke[uredi | uredi kod]
Arteriogeneze je mehanički posredovan proces, izazvan brojnim stresnim reakcijama. Na primer, u slučaju hemodinamski relevantne stenoze u nekom glavnom arterijskom krvnom sudu odgovornom za ishranu nekog tkiva, gradijent pritiska se menja što pokreće rekaciju kolateralnih krvnih sudova. Zbog smanjenja arterijskog pritiska distalno od stenoze, protok krvi se raspodeljuje kroz arteriola koje sada povezuju delove cirkulacije sa visokim pritiskom sa delovima pod niskim pritiskom.[31][32] Ovo rezultuje povećanjem brzine protoka krvi, ali i povećanim otporom i trenjem u kolateralnim arterijama, što dovodi do značajne aktivacije endotela, ushodne regulacije molekula ćelijske adhezije, i povećane aktivnost monocita, koji se transformišu u makrofage. Nakon toga, javlja se još nekoliko morfoloških i vaskularnih promena.[31][33]
Različiti faktori rasta i hemokina su uključeni u angiogenezu i arteriogenezu kao što su;[31][34] VEGF, TGF-α,, i kiseli faktor rasta fibroblasta (a-FGF) u angiogenezi, i GM-CSF, monocitni hemoatraktantni protein-1 (MCP-1) i TGF-β u arteriogenezi. Neki od faktora rasta igraju ulogu u oba procesa: npr b-FGF i PDGF (engl. platelet-derived growth factor ili iztrombocita - izveden faktor rasta).[31] U ishemijskom tkivu, dokazana je i poboljšana ekspresija nekoliko angiogenih faktora i njihovih receptora.[34]
Nasuprot, oslabljenoj cirkulaciji kolaterala u drugim bolestima u šećernoj bolesti, hiperlipidemiji, i starenje ovaj proces je povezan sa smanjenom ekspresijom angiogenskih faktora.[35]
Nekoliko studija pokazalo je i povećanje nivoa cirkulišućih angiogenih faktora kod pacijenata sa ishemijskom bolešću srca, moždanim udarom, ili ishemijom u ekstremitetima, verovatno kao odgovor na tkivnu ishemiju i povredu.[36]
Sasajama je sa svojim saradnicima (početkom devedesetih godina 20. veka)[37] primetio da su masne ćelije povezane sa neovaskularizacijom, povećanjem endotelijalnih migracija ovih ćelija, kao najranijeg događaja u formiranju kapilarne izdanka. On je čak predložili primenu lečenja ishemijske bolesti srca lekovima (heparin) koji promovišu razvoj kolateralne koronarne cirkulacije. Od tada, ovaj koncept terapijske angiogeneze i arteriogeneze sve je više privlačio pažnju istraživača.[31]
Zanimljivi rezultati su nedavno objavljeni na osnovu primene terapijske angiogeneze u perifernoj arterijskoj bolesti, unapređenjem razvoja kolaterala kroz ordiniranje angiogenih faktora rasta.[38][39][40]
U ishemijskoj bolesti srca, u ranim studijama, u kojima su korišćeni rekombinantni proteini, ili geni koji kodiraju za vaskularne faktore rasta, i pokazale ohrabrujuće rezultate u promeni kliničke slike nabolje, što se ogleda u blagom poboljšanju perfuziji srčanog mišića u tretiranoj oblasti. Međutim, u nakim studijama nije dokazan efekat pvog tretmana.[31]
Perspektiva[uredi | uredi kod]
Do sada objavljeni rezultati o uspešnoj genskoj terapiji u prevenciji kardiovaskularnih bolesti, obećavaju, da bi metoda razvoja kolaterala mogle biti primenjena i u terapiji zasnovanoj na primeni angiogenih faktora rasta. Međutim nedovoljna saznanja o ovoj problematici nameće potrebu za još više kardiovaskularnih studija, koje kao krajnji cilj treba da imaju dugoročno praćenje razvoja kolateralnih krvnih sudova, kako bi se utvrdilo u kojoj meri njihovo stanje i funkcija može poslužiti za:
- praćenje vaskularnih bolesti
- kao prognostička determinanta, mogućeg vaskularnog ishoda.
Takođ istraživanjima je potrebno utvrdi i mesto kolaterala u mehanizmima koji dovodi do ishemijskih događaja kod bolesnika sa značajnim aterosklerotskim promenama.
Sve napred navedeno ukazuje na nove prrspektive za prevenciju ponovnog vaskularnog događaja (recidiva) u bolesnika koji boluju od kardiovaskularnih bolesti ili za sprečavanje neželjenog događaja u onih sa naprednom koronarnom aterosklerozom.[41]
Vidi još[uredi | uredi kod]
Napomene[uredi | uredi kod]
- ↑ Subendokardne kolaterala srca, mogu se formirati na ovaj način.
Izvori[uredi | uredi kod]
- ↑ Tayebjee MH, Lip GY, MacFadyen RJ. Collateralization and the response to obstruction of epicardial coronary arteries. QJM. 2004 May;97(5):259-72. Review. PMID 15100419. Free Full Text.
- ↑ 2,0 2,1 2,2 2,3 Ivanović V, Jelkić N, Bikicki M, Petrović M, Čanji T, Srdanović I. Značaj koronarne kolateralne cirkulacije u očuvanju funkcije miokarda. Medicinski pregled. 2007; 60(5-6):287-291.
- ↑ Gaziano JM, Ridker PM, Libby P. Primary and secondary prevention of coronary heart disease. In: Bonow RO, Mann DL, Zipes DP, Libby P,eds. Braunwald's Heart Disease: A Textbook of Cardiovascular Medicine. 9th ed. Philadelphia, Pa: Saunders Elsevier; 2011:chap 49.
- ↑ Greenland P, Alpert JS, Beller GA, et al. 2010 ACCF/AHA guideline for assessment of cardiovascular risk in asymptomatic adults: a report of the American College of Cardiology Foundation/American Heart Association Task Forceon Practice Guidelines. Circulation. 2010;122(25)e584-e636.
- ↑ Hansson GK, Hamsten A. Atherosclerosis, thrombosis, and vascular biology. In: Goldman L, Schafer AI, eds. Cecil Medicine. 24th ed. Philadelphia, PA: Saunders Elsevier; 2011:chap 70.
- ↑ Mosca L, Benjamin EJ, Berra K, et al. Effectiveness-Based Guidelines for the Prevention of Cardiovascular Disease in Women--2011 Update:a guideline from the American Heart Association. Circulation.2011;123(11);1243-1262.
- ↑ Rado Starc, Collaterals of the coronary arteries, MED RAZGL 1995;34 [1] Arhivirano 2014-02-02 na Wayback Machine-u Pristupljeno: 21.1.2014.
- ↑ Rubanyi, G.M. (Ed): Angiogenesis in health and disease. M.Dekker, Inc., New York – Basel, 2000
- ↑ Raizada, M.K., Paton, J.F.R., Kasparov, S., Katovich, M.J. (Eds): Cardiovascular genomics. Humana Press, Totowa, N.J., 2005
- ↑ Kornowski, R., Epstein, S.E., Leon, M.B.(Eds.): Handbook of myocardial revascularization and angiogenesis. Martin Dunitz Ltd., London, 2000
- ↑ Stegmann, T.J.: New Vessels for the Heart. Angiogenesis as New Treatment for Coronary Heart Disease: The Story of its Discovery and Development. Henderson, Nevada: CardioVascular BioTherapeutics Inc., 2004
- ↑ Laham, R.J., Baim, D.S.: Angiogenesis and direct myocardial revascularization. Humana Press, Totowa, NJ, 2005
- ↑ (bg) Anastomoza, definicija pojma na: www.puls.bg Pristupljeno 10.1.2014.
- ↑ James TN Anatomy of the coronary arteriae. New York;Paul B.Hoeber; 1961
- ↑ Baroldi G. Scomazzoni G. Coronary circulation in the normal and the patologic heart. Waschington: Office of the Surgeon General Department of the Army; 1967.
- ↑ Schaper W, The collateral circulation of the heart, New York, N.Y.: Elsevier, 1971.
- ↑ Kolibash AJ, et al., Coronary collateral vessels: spectrum of physiologic capabilities with respect to providing rest and stress myocardial perfusion, maintenance of left ventricular function, and protection against infarction, American Journal of Cardiology 1982; 50: 230-238.
- ↑ See notes 5-15 in Kolibash, op. cit., for relevant studies with this perspective. (Note that the most recent is from 1977.)
- ↑ Kolibash, op. cit., 232. See also Yamagsihi M, The functional significance of transient collaterals during coronary artery spasm American Journal of Cardiology 1985; 56: 407-12.
- ↑ 20,0 20,1 Meier B, Luethy P. Coronary wedge pressure as predictor of recruitable collateral arteries. Circulation 1984; 70: II–266.
- ↑ 21,0 21,1 21,2 Braunwald E, Sobel BE. Coronary blood flow and myocardial ischemia. In: Braunwald E, ed. Heart disease. A textbook of cardiovascular medicine. Philadelphia: WB Saunders, 1992: 1161–99.
- ↑ James TN. Anatomy of arteries and veins. In: Hurst JW, Logue RB, Schlant RC, Wenger NK, eds. The Heart, arteries and veins. New York: McGraw-Hill, 1978: 32–47.
- ↑ Verani MS. The functional significance of coronary collateral vessels: anecdote confronts science. Cathet Cardiovasc Diagn 1983; 9: 333–7.
- ↑ Arthur C. Guyton Medicinska fiziologija, Medicinska knjiga-Beograd-Zagreb 1990
- ↑ Rahimtoola SH. A perspective on the three large multicenter randomized clinical trials of coronary bypass surgery for chronic stable angina. Circulation 1985; 72: Suppl 5: 123–35.
- ↑ Rahimtoola SH. The hibernating myocardium. Am H J 1989; 17: 211–21.
- ↑ Starc R. Uspavana sršna mišica. Med Razgl 1991; 30: 259–62.
- ↑ Ivanović V, Jelkić N, Bikicki M, Petrović M, Čanji T, Srdanović I. Značaj koronarne kolateralne cirkulacije u očuvanju funkcije miokarda. Medicinski pregled. 2007; 60(5-6):287-291. SCIndeks-srpski nacionalni citatni indeks[mrtav link] Posećeno 11. januara 2011.
- ↑ Rahimtoola SH. A perspective on the three large multicenter randomized clinical trials of coronary bypass surgery for chronic stable angina. Circulation 1985; 72: Suppl 5: 123–35.
- ↑ Billinger M. et all, Physiologically assessed collateral flow and adverse cardiac ischemic events:a follow-up study in 403 patints with coronary artey diseasse. J Am.Coll Cardiol. 2010;40:1545-50
- ↑ 31,0 31,1 31,2 31,3 31,4 31,5 van Royen N, Piek JJ, Buschmann I, et al. Stimulation of arteriogenesis: a new concept for the treatment of arterial occlusive disease. Cardiovasc Res.2001; 49: 543–553.
- ↑ Spalteholz W. Die Koronararterien des Herzens. Verhandl Anat Ges. 1907;21:141; in Anat Anz 30.
- ↑ Fulton WFM. The Coronary Arteries. Springfield, Ill: Charles C Thomas Publishers; 1965.
- ↑ 34,0 34,1 Connolly D. Vascular permeability factor: a unique regulator of blood vessel function. J Cell Biochem. 1991;47:219-223.
- ↑ Rak JW, St Croix BD, Kerbel RS. Consequences of angiogenesis for tumor progression, metastasis and cancer therapy. Anticancer Drugs. 1995;6:3-18.
- ↑ Kastrup J, Jorgensen E, Drvota V. Vascular growth factor and gene therapy to induce new vessels in the ischemic myocardium: therapeutic angiogenesis.Scand Cardiovasc J. 2001; 35: 291–296.
- ↑ Sasayama S, Fujita M. Recent insights into coronary collateral circulation. Circulation. 1992; 85: 1197–1204.
- ↑ Lederman RJ, Mendelsohn FO, Anderson RD, et al. Therapeutic angiogenesis with recombinant fibroblast growth factor-2 for intermittent claudication (the TRAFFIC study): a randomised trial. Lancet. 2002; 359:2053–2058.CrossRefMedline
- ↑ Donnelly R, Yeung JM. Therapeutic angiogenesis: a step forward in intermittent claudication. Lancet. 2002; 359: 2048–2050.CrossRefMedline
- ↑ Warren RS, Yuan H, Matli MR, Gillett NA, Ferrara N. Regulation by vascular endothelial growth factor of human colon cancer tumorigenesis in a mouse model of experimental liver metastasis. J Clin Invest. 1995;95:1789-1797.
- ↑ Wolfgang Schaper, Wulf D. Ito, Molecular Mechanisms of Coronary Collateral Vessel Growth, Circulation Research. 1996; 79: 911-919 doi: 10.1161/01.RES.79.5.911 Full Text Pristupljeno 21.1.2014.