Hiralnost molekula
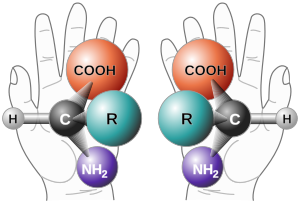

Hiralnost molekula je osobina koja se može često naći kod organskih jedinjenja kao što su alkoholi, aldehidi, kiseline, ugljeni hidrati, proteini itd. Svaka organska supstanca koja je hiralna pokazuje optičku aktivnost. Za molekul kažemo da je hiralan ako nema unutrašnju simetriju i ako se ne može poklopiti sa svojim likom u ogledalu.
Optička aktivnost[uredi | uredi kod]
Za neku supstancu kažemo da je optički aktivna ako ima osobinu da obrće ravan polarizovane svjetlosti koja se propušta kroz tu supstancu. Ravan se obrće za neki ugao koji može biti u smjeru kazaljke na satu ili suprotnom smjeru. Polarizovna svjetlost je monohromatska svjetlost čije se oscilacije vrše samo u jednoj ravni normalnoj na pravac prostiranja.
Objašnjenje pojma hiralnosti[uredi | uredi kod]
Kod atoma ugljenika koji gradi četiri jednostruke veze dolazi do sp3 hibridizacije, pri čemu su četiri sp3 hibridne orbitale raspoređene tetraedarski u prostoru. U slučaju molekula u kome ugljenik gradi četiri jednostruke veze, atomi ili atomske grupe koje se vezuju sa atom ugljenika su raspoređene u prostoru tetraedarski, tj. atom ugljenika se nalazi u centru tetraedra, a atomske grupe na vrhovima tog tetraedra. Ako su za atom ugljenika vezane bar dvije iste atomske grupe, onda koje god kombinacije se naprave spajajući atomske grupe sa atomom ugljenika dobiće se molekuli koji se mogu poklopiti tj. prostorno su identični. Ako je atom ugljenika vezan za četiri različite atomske grupe, onda su moguća dva različita prostorna rasporeda u molekulu, i pri tome se ta dva rasporeda odnose kao lik i slika u ogledalu. Oba molekula imaju identičnu strukturu ali različit prostorni raspored, i oni predstavljaju prostorne izomere ili stereoizomere. Ova dva izomera se nazivaju enantiomeri, tj. enantiomerni oblici neke organske supstance.
Ugljenikov atom za koji u vezane četiri različita atoma ili atomske grupe se naziva hiralni ili asimetrični C-atom.
Bitno je istaći i da na hiralnost utiču i izotopi, tako npr. atom vodonika (1H) i atom deuterijuma (2H) predstavljaju dva različita supstituenta na hiralnom atomu, i na taj način se od nehiralnog molekula može dobiti hiralni.
Postoje i molekuli koji ne posjeduju hiralni centar tj. atom ali posjeduju hiralnost zbog specifičnog rasporeda atomskih grupa u molekulu. Postoje i molekuli koji posjeduju hiralni centar ali ne posjeduju hiralnost zbog toga što molekul kao cjelina posjeduje neku ravan simetrije.
Dva enantiomerna oblika neke supstance imaju iste fizičke osobine kao što je tačka ključanja, rastvorljivost, gustina itd., jedina razlika se sastoji u optičkoj aktivnosti. Zbog toga se ovaj tip izomerije naziva i optička izomerija. Dva enantiomera imaju istu apsolutnu vrijednost rotacije ravni svjetlosti, samo je smjer različit.
Što se tiče hemijske reaktivnosti, dva enantiomera pokazuju istu hemijsku reaktivnost prema ahiralnim reagensima, međutim pri reakcijama sa hiralnim supstancama se ponašaju različito. Mnoge organske i biohemijske reakcije su stereoselektivne i mnogi enzimi su hiralni i ponašaju se različito prema dva enantimoera.
Nomenklatura[uredi | uredi kod]
Postoji više načina za označavanje enantiomera jedne supstance, tj. za označavanje različitih stereoizomera neke supstance. Kao standard za D L označavanje je uzet gliceraldehid (HOCH2CHOHCHO), pri čemu je usvojeno da se (+) gliceraldehid označava kao D oblik a (-)gliceraldehid kao L oblik. Označavanje ostalih supstanci koje imaju enantiomere tj. čiji molekuli posjeduju hiralnost se označavaju na osnovu upoređivanja sa gliceraldehidom.
(+) ili (-) način označavanja entantiomera ne govori o konfiguraciji na hiralnom atomu, nego se označavaju na osnovu optičke aktivnosti tj. zavisno u kojem se pravcu obrće ravan polarizovane svjetlosti.
Postoji i R S sistem označavanja koji se zasniva na određivanju apsolutnih konfiguracija hiralnih molekula. Kod ovog sistema ne postoje referentni molekuli, i predstavlja najprecizniji sistem označavanja a zasniva se na CIP pravilima.
Racemat[uredi | uredi kod]
Jedan entantiomer može da pređe u drugi samo ako dođe do raskidanja i ponovnog stvaranja hemijskih veza. Ekvimolekulska smješa dva enantiomera se naziva racemat i obilježava se sa (+)(-) ili DL. Racemska smješa nije optički aktivna jer se rotacije entantiomera međusobno potiru.
Hiralni molekuli se u prirodi rijetko nalaze u obliku racemata, najčešće se nalaze kao samo jedan enantiomer.
Pri hemijskim reakcijama pri kojima postaje hiralni atom, gotovo uvijek nastaju racemati. Mnogi organski molekuli imaju i više hiralnih atoma i mogu postojati u više prostornih oblika, ali u prirodi se najčešće nalati samo jedan oblik.
Sve prirodne aminokiseline imaju L konfiguraciju. Svi ugljeni hidrati imaju D konfiguraciju.
